
科目: 来源: 题型:选择题
| A. |  验证酸性:H2CO3>H2SiO3 | B. | 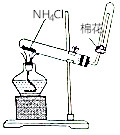 实验室制取氨气 | ||
| C. |  证明石蜡油分解生成的气体是乙烯 | D. | 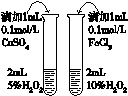 比较不同催化剂对反应速率的影响 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 相同温度下,0.6mol/L氨水溶液与0.3mol/L氨水溶液中c(OH-)之比是2:1 | |
| B. | 将稀氨水逐滴加入稀硫酸中,当溶液的pH=7时,c(SO42-)>c(NH4+) | |
| C. | 25℃时,10mL 0.02mol•L-1HCl溶液与10mL0.02mol•L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20mL,则溶液的pH=12 | |
| D. | 25℃时pH=10的NaOH溶液与60℃时pH=10的NaClO溶液中:c(H+)相等 |
查看答案和解析>>
科目: 来源: 题型:推断题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 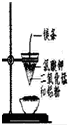 可制得金属锰,用同样的装置可制得金属铬 | |
| B. |  制取少量氨气 | |
| C. | 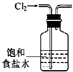 除去Cl2中的少量HCl | |
| D. |  制乙酸乙酯 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 乙炔和苯 | B. | 甲烷和乙烷 | C. | 乙烯和丁炔 | D. | 苯和苯乙烯 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 当生成的沉淀量达到最大时,消耗NaOH溶液的体积V≥100 mL | |
| B. | 当金属全部溶解时,参加反应的硝酸的物质的量一定是0.4mol | |
| C. | 参加反应的金属的总质量为9.6 g>m>3.6 g | |
| D. | 当金属全部溶解时收集到NO气体的体积一定为2.24 L |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Fe-2e-═Fe2+ | B. | 2H2O+O2+4e-═4OH- | ||
| C. | 2H++2e-═H2↑ | D. | 4OH--4e-═2H2O+O2↑ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 滴加甲基橙试液显红色的溶液Fe3+、NH4+、SCN- | |
| B. | pH值为1的溶液Cu2+、Na+、Mg2+、NO3- | |
| C. | 水电离出来的c(H+)=10-13mol/L的溶液K+、HCO3-、Br-、Ba2+ | |
| D. | 所含溶质为Na2SO4的溶液K+、HCO3-、NO3-、Al3+ |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 向CaCl2溶液中通入过量CO2 | B. | 向水玻璃溶液中通入过量CO2 | ||
| C. | 向澄清石灰水中通入过量CO2 | D. | 向水玻璃溶液中加入过量盐酸 |
查看答案和解析>>
科目: 来源: 题型:实验题
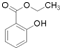 )广泛用于黑醋栗酒、依兰、百合等的花香型的调和香料,还用作草莓等果香香精及化工行业.水杨酸乙酯为无色油状液体,呈淡的冬青油香气,沸点233℃,溶于乙醇、乙醚,微溶于水和甘油.利用水杨酸(沸点:211℃)、乙醇(沸点:78.4℃)和浓硫酸在硫酸铝存在下于100℃下酯化而成,反应方程式如下:
)广泛用于黑醋栗酒、依兰、百合等的花香型的调和香料,还用作草莓等果香香精及化工行业.水杨酸乙酯为无色油状液体,呈淡的冬青油香气,沸点233℃,溶于乙醇、乙醚,微溶于水和甘油.利用水杨酸(沸点:211℃)、乙醇(沸点:78.4℃)和浓硫酸在硫酸铝存在下于100℃下酯化而成,反应方程式如下: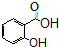 +C2H5OH?
+C2H5OH?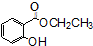 +H2O
+H2O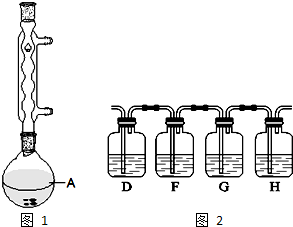
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com