
科目: 来源: 题型:选择题
| A. | 两种烃相对分子质量相同,但结构不同,性质也不同,一定是同分异构体 | |
| B. | 两种有机物若互为同分异构体,则它们一定不互为同系物 | |
| C. | 分子组成相差一个或几个CH2原子团的化合物必定互为同系物 | |
| D. | 两种烃所含有碳元素的质量分数相同,一定互为同分异构体 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | B. | 碱性:KOH>NaOH>Mg(OH)2>Al(OH)3 | ||
| C. | 热稳定性:H2S>H2O>PH3>NH3 | D. | 原子半径:Na>S>O>F |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
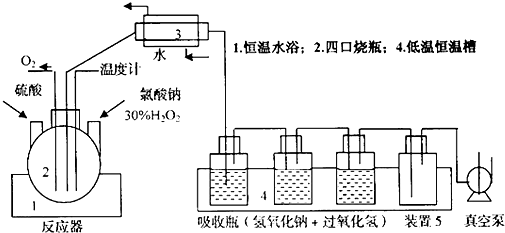
查看答案和解析>>
科目: 来源: 题型:实验题
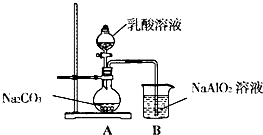 乳酸(2-羟基丙酸)为无色液体,与水混溶,弱挥发性.它在多种生物化学过
乳酸(2-羟基丙酸)为无色液体,与水混溶,弱挥发性.它在多种生物化学过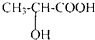
| 次数 | 1 | 2 | 3 | 4 |
| 滴定体积(mL) | 19.22 | 19.18 | 19.80 | 19.20 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com