
科目: 来源: 题型:选择题
| A. | 正极发生的电极反应为H2O2+2H++2e-═2H2O | |
| B. | 电池总反应为Mg+H2O2═Mg(OH)2 | |
| C. | 工作时,正极周围海水的pH减小 | |
| D. | 电池工作时,溶液中的H+向负极移动 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 第VⅡA族元素形成的氢化物中沸点最高的是HI | |
| B. | 水分子很稳定性是因为水分子间易形成氢键 | |
| C. | 二氧化碳电子式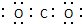 | |
| D. | 第三周期元素形成的简单离子中,半径最小的是Al3+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氯化氢的摩尔质量等于NA个氯化氢分子的质量 | |
| B. | 常温常压下1mol二氧化碳的体积大于22.4L | |
| C. | 64g金属铜发生氧化反应,一定失去2NA个电子 | |
| D. | 62g氧化钠溶于水后,所得溶液中含有NA个O2-离子 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 溶液的pH增大 | B. | 锌片的质量减轻 | ||
| C. | 溶液中的SO42-浓度增大 | D. | 溶液的密度增大 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 锌粒与稀硝酸的反应 | |
| B. | 灼热的木炭与CO2的反应 | |
| C. | 过氧化钠与水的反应 | |
| D. | Ba(OH)2•8H2O晶体与NH4Cl晶体的反应 |
查看答案和解析>>
科目: 来源: 题型:解答题
 ,反应类型:加聚反应(或聚合反应)
,反应类型:加聚反应(或聚合反应) 反应类型:取代反应
反应类型:取代反应查看答案和解析>>
科目: 来源: 题型:推断题
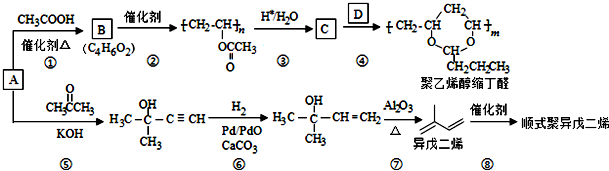
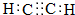 ,B含有的含氧官能团是酯基(写名称).
,B含有的含氧官能团是酯基(写名称).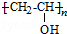 ,D为CH3CH2CH2CHO.
,D为CH3CH2CH2CHO.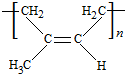 .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 稀释后溶液的pH=9 | |
| B. | 稀释过程中,溶液中所有离子的浓度均减小 | |
| C. | 稀释后溶液中$\frac{c(N{H}_{4}^{+})}{c(N{H}_{3}•{H}_{2}O)}$ 减小 | |
| D. | 该氨水稀释前后中和盐酸的能力相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com