
科目: 来源: 题型:选择题
| A. | 分子中C、H、O个数之比为1:2:3 | B. | 分子中C、H个数之比为1:2 | ||
| C. | 分子中一定含有氧原子 | D. | 此有机物的最简式为CH2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,1L C2H5OH完全燃烧后生成的CO2分子个数约为NA/11.2 | |
| B. | 18g 50%的遮糖水溶液中原子总数约为1.6 NA | |
| C. | 0℃、101KPa下,4.48LNH3中共用电子对数为0.6NA | |
| D. | 将lmol Cl2通入水中,HClO、Cl-、ClO- 粒子数之和为2NA |
查看答案和解析>>
科目: 来源: 题型:推断题
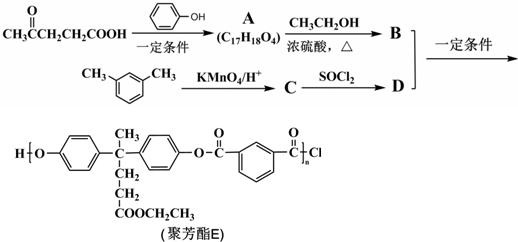
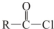 +R′OH→
+R′OH→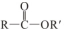 +HCl
+HCl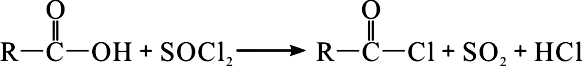
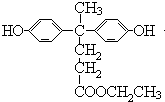 .
. .
. 的路线.
的路线.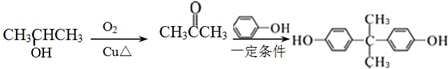 .
.查看答案和解析>>
科目: 来源: 题型:填空题
 .
.查看答案和解析>>
科目: 来源: 题型:实验题
查看答案和解析>>
科目: 来源: 题型:选择题
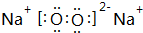
| A. | 甲基的电子式 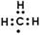 | |
| B. | 乙醛的结构简式为CH3COH | |
| C. | 按系统命名法,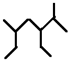 的名称为2,5-二甲基-3-乙基庚烷 的名称为2,5-二甲基-3-乙基庚烷 | |
| D. | 邻甲基苯酚的结构简式为 |
查看答案和解析>>
科目: 来源: 题型:实验题

| 试管编号 | 0.01mol/LKMnO4 | 0.5mol/LH2SO4 | 0.2mol/LH2C2O4 | H2O | 褪色时间/s |
| ① | 4mL | 5mL | 2mL | VmL | t1 |
| ② | 4mL | 5mL | 4mL | 7mL | t2 |
| ③ | 4mL | 5mL | 6mL | 5mL | t3 |
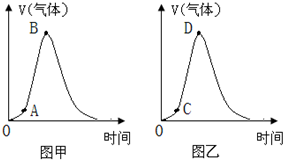
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:解答题
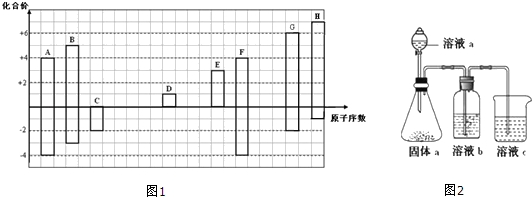
 .
. .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2++2OH-$\stackrel{水溶加热}{→}$CH3COONH4+3NH3+2Ag↓+H2O | |
| B. | 苯酚钠溶液中通入少量CO2:CO2+H2O+2C6H5O-→2C6H5OH+CO32- | |
| C. | 氯乙烷中滴入AgNO3溶液检验其中氯元素:Cl-+Ag+═AgCl↓ | |
| D. | 硫酸铝溶液中加入过量的氨水:Al3++3NH3•H2O═Al(OH)3↓+3NH4+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com