
科目: 来源: 题型:推断题



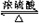 CH3COOCH2CH3+H2O;反应类型:酯化反应.
CH3COOCH2CH3+H2O;反应类型:酯化反应. ;反应类型:加聚反应.
;反应类型:加聚反应.查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:实验题
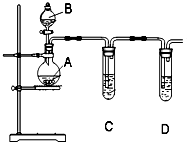 某化学实验小组选用图所示装置和下列所给试剂来证明非金属性:Cl>I.
某化学实验小组选用图所示装置和下列所给试剂来证明非金属性:Cl>I.查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H2O2的电子式: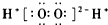 | |
| B. | CO2分子的结构式:O═C═O | |
| C. | 原子核内有8个中子的碳原子:${\;}_8^{14}C$ | |
| D. | 氯化钾的分子式:KCl |
查看答案和解析>>
科目: 来源: 题型:实验题
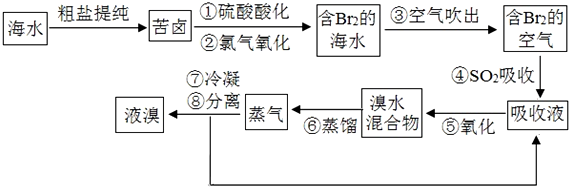
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 一定存在SO42-、NH4+、Cl-,一定不存在CO32- | |
| B. | c(SO42-)=0.1mol•L-1,c(Cl-)>c(SO42-) | |
| C. | 一定存在SO42-、CO32-、NH4+,可能存在Na+ | |
| D. | 一定存在SO42-、NH4+,可能存在Na+、Cl- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③⑧ | B. | ②③④ | C. | ①④⑥ | D. | ④⑤⑦ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | X-二氧化硫,Y-氢氧化钠溶液 | B. | X-氢氧化钠溶液,Y-硫酸铝溶液 | ||
| C. | X-二氧化碳,Y-偏铝酸钠溶液 | D. | X-二氧化碳,Y-饱和碳酸钠溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com