
科目: 来源: 题型:选择题
| A. | ①②③④⑤⑥ | B. | 仅①②③④⑤ | C. | 仅①②③④ | D. | 仅①②③ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将胆矾加热除去结晶水后,称取16g溶解在1L水中 | |
| B. | 称取25g胆矾溶于水,然后将此溶液稀释至1L | |
| C. | 称取25g胆矾溶解在1L水里 | |
| D. | 将16g胆矾溶于水,然后将此溶液稀释至1L |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ③⑥ | B. | ②③ | C. | ①④ | D. | ⑤⑥ |
查看答案和解析>>
科目: 来源: 题型:选择题
| 对二甲苯 | 邻二甲苯 | 间二甲苯 | 苯 | |
| 沸点/℃ | 138 | 144 | 139 | 80 |
| 熔点/℃ | 13 | 25 | 47 | 6 |
| A. | 该反应属于取代反应 | |
| B. | 用蒸馏的方法可将苯从反应所得产物中首先分离出来 | |
| C. | 甲苯的沸点高于144℃ | |
| D. | 从二甲苯混合物中,用冷却结晶的方法可将对二甲苯分离出来 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 正极反应式:Ag+Cl--e-=AgCl | |
| B. | 每生成1 mol Na2Mn5O10转移2 mol电子 | |
| C. | Na+不断向“水”电池的负极移动 | |
| D. | AgCl是还原产物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 14 g乙烯和丙烯混合气体中的氢原子数为2NA | |
| B. | 1 molN2与4 molH2反应生成的NH3分子数为2NA | |
| C. | 铜-锌(稀硫酸)原电池,每转移数2NA电子则正极消耗1 mol铜 | |
| D. | 标准状况下,2.24 LCCl4含有的共价键数为0.4NA |
查看答案和解析>>
科目: 来源: 题型:选择题
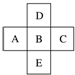
| A. | 5x+10 | B. | 5x | C. | 5x+14 | D. | 5x+16 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 全部 | B. | ①②③④ | C. | ①②③⑤ | D. | ①②④⑤ |
查看答案和解析>>
科目: 来源: 题型:解答题
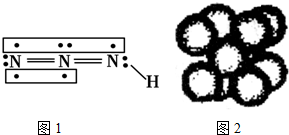
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.004(mol•L-1•min-1) | B. | 0.008(mol•L-1•min-1) | ||
| C. | 0.016(mol•L-1•min-1) | D. | 0.032(mol•L-1•min-1) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com