
科目: 来源: 题型:实验题
| 编号 | 电极材料 | 电解质溶液 | 电流指针偏转方向 |
| 1 | Mg Al | 稀盐酸 | 偏向Al |
| 2 | Al Cu | 稀盐酸 | 偏向Cu |
| 3 | Al 石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg Al | NaOH溶液 | 偏向Mg |
| 5 | Al Zn | 浓硝酸 | 偏向Al |
 .
.查看答案和解析>>
科目: 来源: 题型:选择题
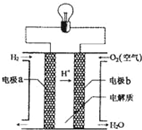 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法正确的是( )| A. | 该电池工作时电能转化为化学能 | |
| B. | 该电池中电极a是正极 | |
| C. | 外电路中电子由电极a通过导线流向电极b | |
| D. | 该电池的总反应:H2+O2═H2O |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验题
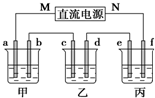 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题:
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放足量的NaCl溶液、AgNO3溶液、x溶液,a、b、c、d电极均为石墨电极.接通电源,经过一段时间后,乙中c电极质量增加.据此回答问题:查看答案和解析>>
科目: 来源: 题型:实验题
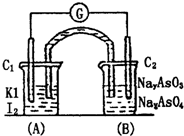 已知反应AsO43-+2I-+H+?AsO33-+I2+H2O是可逆反应.设计如图装置,进行下述操作:
已知反应AsO43-+2I-+H+?AsO33-+I2+H2O是可逆反应.设计如图装置,进行下述操作:查看答案和解析>>
科目: 来源: 题型:实验题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Pb为正极被氧化 | B. | SO42-只向PbO2极移动 | ||
| C. | 电解质溶液密度不断减小 | D. | 电解质溶液浓度不变 |
查看答案和解析>>
科目: 来源: 题型:填空题
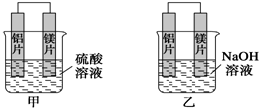
 某同学用铁、铜作为电极,稀硫酸作为电解液组成原电池,如图所示,完成下列空格.(涉及到电极填写具体物质的元素符号)
某同学用铁、铜作为电极,稀硫酸作为电解液组成原电池,如图所示,完成下列空格.(涉及到电极填写具体物质的元素符号)查看答案和解析>>
科目: 来源: 题型:实验题
 图为实验室制取某有机物的装置图,试通过已学知识回答下列问题:
图为实验室制取某有机物的装置图,试通过已学知识回答下列问题: .
.查看答案和解析>>
科目: 来源: 题型:填空题
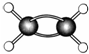 科学家致力于二氧化碳的“组合转化”技术的研究,把过多二氧化碳转化为有益于人类的物质.
科学家致力于二氧化碳的“组合转化”技术的研究,把过多二氧化碳转化为有益于人类的物质. 代表氢原子,
代表氢原子, 代表碳原子)和水,该有机物的结构简式为CH2=CH2.
代表碳原子)和水,该有机物的结构简式为CH2=CH2.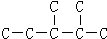 ,该烷烃的名称为2,3-二甲基戊烷;其一溴代物有6种.
,该烷烃的名称为2,3-二甲基戊烷;其一溴代物有6种.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com