
科目: 来源: 题型:解答题
 .
.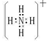 .
.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| 加入试剂 | 对应化学或离子方程式 | ||
| A | 乙烷(乙烯) | 氢气 | CH2=CH2+H2$→_{加热}^{Ni}$CH3CH3 |
| B | CH3COOC2H5(CH3COOH) | NaOH溶液 | CH3COOH+NaOH=CH3COONa+H2O |
| C | MgCl2( FeCl3) | 氨水 | Fe3++3NH3•H2O=Fe(OH)3↓+3NH4+ |
| D | Fe2+(Fe3+) | Fe粉 | 2Fe3++Fe=3Fe2+ |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 第七周期有50种元素 | B. | 该原子的质量数为184 | ||
| C. | 该元素的相对原子质量为298 | D. | 该原子核外有114个电子 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验步骤 | 实验现象 |
| ①取少量该溶液,加入NaOH溶液 | 有白色沉淀生成,当NaOH过量时,沉淀部分溶解 |
| ②取少量该溶液,加入铜片和浓硫酸,加热 | 有无色气体产生,遇空气可以变成红棕色 |
| ③取少量该溶液,加入BaCl2溶液 | 有白色沉淀生成 |
| ④取③中的上层清液,加入AgNO3溶液 | 有稳定的白色沉淀生成,且不溶于稀硝酸 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ${\;}_{2}^{3}$He的最外层电子数为2,具有较强的金属性 | |
| B. | ${\;}_{2}^{3}$He位于周期表第二周期第ⅡA族 | |
| C. | 其原子核中质子数为2、中子数为1 | |
| D. | 核聚变是通过化学反应而释放出的能量 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 密度 (g•mL-1) | 熔点 (℃) | 沸点 (℃) | 溶解性 | |
| 苯甲酸 | 1.2659 | 122.13 | 249 | 微溶于水,易溶于乙醇、乙醚等有机溶剂 |
| 苯酚 | 1.07 | 40.6 | 181.9 | 易溶于乙醇、乙醚,65℃以上能与水互溶 |
| 乙醇 | 0.79 | -114.3 | 78.5 | 与水混溶,可混溶于醚、氯仿、甘油等多数有 机溶剂 |
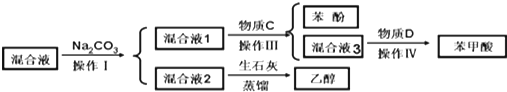
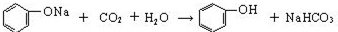 .
.| 实验步骤 | 现象和结论 |
| ①取少量混合液1于试管,滴加BaCl2, 振荡,静置 | 产生白色沉淀,BaCO3 |
| ②取少量步骤①上层清夜于试管,滴加0.1mol/L盐酸再将产生的气体通入澄清石灰水中 | 澄清石灰水变浑浊 说明混合液1含有HCO3- |
| ③另取少量混合液1于试管,滴加0.1mol/L FeCl3溶液,振荡 | 溶液不显紫色, 说明混合液1不含有酚羟基 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com