
科目: 来源: 题型:选择题
| A. | 正反应的速率为零 | B. | SO2完全转化为SO3 | ||
| C. | SO3的物质的量浓度不再变化 | D. | SO2、O2和SO3的物质的量浓度相等 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | υ(W)=3υ(Z) | B. | 3υ(X)=2υ(Z) | C. | υ(X)=2υ(Y) | D. | 3υ(W)=2υ(X) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 9.0 | B. | 0.9 | C. | 0.45 | D. | 4.5 |
查看答案和解析>>
科目: 来源: 题型:解答题
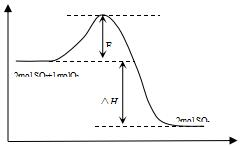 2SO2(g)+O2(g)?2SO3(g)△H<0,是工业制硫酸的主要反应之一.
2SO2(g)+O2(g)?2SO3(g)△H<0,是工业制硫酸的主要反应之一.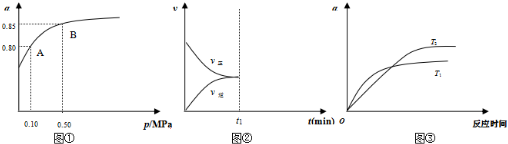
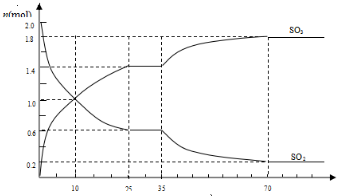
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na+、Fe2+、NO3- | B. | Na+、Mg2+、NO3- | ||
| C. | Cr2O72-、Ba2+、Cl- | D. | K+、Na+、S2O32- |
查看答案和解析>>
科目: 来源: 题型:解答题
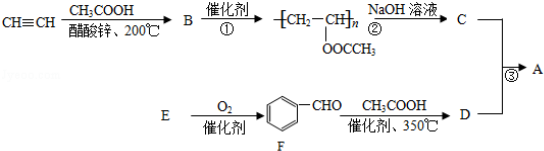

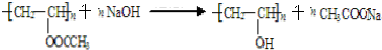 .
. .
. .
.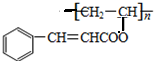 .
.查看答案和解析>>
科目: 来源: 题型:选择题
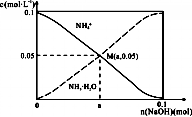 常温下,向1L0.1mol•L-1NH4Cl溶液中,不断加入固体NaOH后,NH4+与NH3•H2O的变化趋势如图所示(不考虑体积变化和氨的挥发),下列说法不正确的是( )
常温下,向1L0.1mol•L-1NH4Cl溶液中,不断加入固体NaOH后,NH4+与NH3•H2O的变化趋势如图所示(不考虑体积变化和氨的挥发),下列说法不正确的是( )| A. | M点溶液中水的电离程度比原溶液小 | |
| B. | 据电荷守恒可知在M点时,n(OH-)-n(H+)=(a-0.05)mol | |
| C. | 当n(NaOH)=0.1mol时,c(Na+)=c(NH4+)+c(NH3•H2O) | |
| D. | 随着NaOH的加入,$\frac{c({H}^{+})}{c(N{H}_{4}^{+})}$不断增大 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com