
科目: 来源: 题型:选择题
| A. | 加入醋酸钠固体 | B. | 加入盐酸 | C. | 加入蒸馏水 | D. | 升高温度 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 绿色荧光蛋白分子中氨基酸排列顺序一定相同 | |
| B. | 绿色荧光蛋白能发生颜色反应及盐析、变性等 | |
| C. | 绿色荧光蛋白可发生水解反应生成多种氨基酸 | |
| D. | 绿色荧光蛋白可用于跟踪生物细胞的分子变化 |
查看答案和解析>>
科目: 来源: 题型:填空题
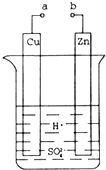 原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置.
原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 一定温度下,反应MgCl2(l)═Mg(l)+Cl2(g)的△H>0△S>0 | |
| B. | 水解反应NH4++H2O?NH3•H2O+H+的△H<0 | |
| C. | 水能、电能、天然气都是可再生能源 | |
| D. | 凡是化合反应都是放热反应,分解反应都是吸热反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 相同质量的CO2(g)和干冰相比较,干冰的能量一定高于CO2(g) | |
| B. | 化学反应过程中能量的变化只可能有吸热和放热两种表现形式 | |
| C. | 同温同压下,反应H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件的△H相同 | |
| D. | 放热的反应在常温下一定能自发进行 |
查看答案和解析>>
科目: 来源: 题型:解答题
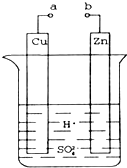 原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置.
原电池是化学对人类的一项重大贡献.某兴趣小组为研究原电池原理,设计如图装置.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.5mol CO+2mol H2O(g)+1mol CO2+1mol H2 | |
| B. | 1 mol CO+1mol H2O(g)+1mol CO2+1mol H2 | |
| C. | 0.5mol CO+1.5mol H2O(g)+0.4mol CO2+0.4mol H2 | |
| D. | 0.5mol CO+1.5mol H2O(g)+0.5mol CO2+0.5mol H2 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1个 | B. | 2个 | C. | 3个 | D. | 4个 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com