
科目: 来源: 题型:多选题

| A. | a 是氧气,b 是甲醇 | |
| B. | 质子从 N 电极区穿过质子交换膜移向 M 电极区 | |
| C. | 正极反应为:O2+2H2O+4e-═4OH- | |
| D. | 当电路中有 3mole-转移时,电池中n(H+)变化为 0 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 气体的密度不再变化 | B. | NH3和 NO 的反应速率相等 | ||
| C. | 反应速率不再变化 | D. | NO 和H2O 浓度比不再变化 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 新方法利用的是化学变化,旧方法利用的是物理变化 | |
| B. | 反应②中既有旧化学键的断裂又有新化学键的形成 | |
| C. | 在反应①中每生成 12g 金刚石需要消耗 46g 金属钠 | |
| D. | 反应①和反应②中所得的金刚石都是还原产物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2Fe3++Cu=2Fe2++Cu 2+ | B. | Cu2++H2S=CuS↓+2H+ | ||
| C. | Cl2+2I-=2Cl-+I2 | D. | Al3++3NH3•H2O=Al(OH)3↓+3NH4+ |
查看答案和解析>>
科目: 来源: 题型:推断题
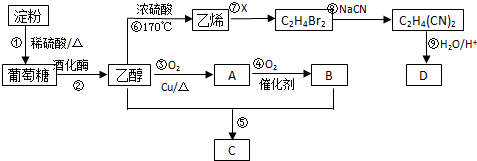
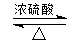 CH3COOCH2CH3+H2O.反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是NaOH溶液.
CH3COOCH2CH3+H2O.反应⑥用于实验室制乙烯,为除去其中可能混有的SO2应选用的试剂是NaOH溶液.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 除②以外 | B. | 除④以外 | C. | 除⑤以外 | D. | 全部正确 |
查看答案和解析>>
科目: 来源: 题型:推断题
| ① | |||||||
| ② | ③ | ④ | |||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
 ,酸性最强的物质的化学式是HClO4,气态氢化物最稳定的物质的化学式是HF.
,酸性最强的物质的化学式是HClO4,气态氢化物最稳定的物质的化学式是HF. .
.查看答案和解析>>
科目: 来源: 题型:实验题
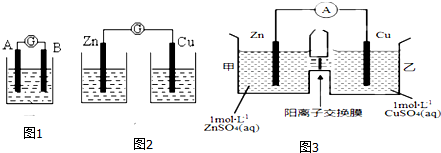
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 4个 | B. | 5个 | C. | 6个 | D. | 7个 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | c的原子半径是这些元素中最大的 | |
| B. | b与其他三种元素均可形成至少两种二元化合物 | |
| C. | a与其他三种元素形成的二元化合物中其化合价均为+1 | |
| D. | d和a形成的化合物的溶液呈弱酸性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com