
科目: 来源: 题型:选择题
| A. | ①③④ | B. | ②④ | C. | ①③ | D. | ①② |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 金属性:K>Na>Li | B. | 酸性:HClO3>H2SO4>H3PO4 | ||
| C. | 还原性:I->Br->Cl- | D. | 氧化性:F2>Cl2>Br2 |
查看答案和解析>>
科目: 来源: 题型:推断题
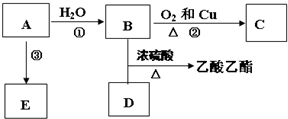
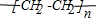 ,E不能(填“能”或“不能”)使酸性KMnO4溶液褪色.
,E不能(填“能”或“不能”)使酸性KMnO4溶液褪色.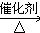 2CH3CHO+2H2O,反应类型氧化反应;B+DCH3COOH+C2H5OH
2CH3CHO+2H2O,反应类型氧化反应;B+DCH3COOH+C2H5OH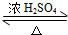 CH3COOC2H5+H2O,反应类型酯化(或取代)反应.
CH3COOC2H5+H2O,反应类型酯化(或取代)反应.查看答案和解析>>
科目: 来源: 题型:实验题
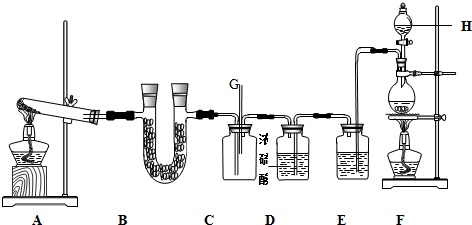
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 水的生成与水的电解是可逆反应 | |
| B. | 实验室用H2O2制O2,加入MnO2后,反应速率明显加快 | |
| C. | 反应2SO2+O2═2SO3中,可以通过改变反应条件让SO2、O2完全转化为SO3 | |
| D. | 金属钠与足量水反应,增加水的量能加快反应速率 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 第IA族元素全部是金属元素 | |
| B. | 过渡元素全是金属元素 | |
| C. | 第ⅦA族元素是同周期中非金属性最强的元素 | |
| D. | 在元素周期表中金属与非金属的分界线附近可以寻找制造半导体的材料 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 乙烯的结构简式为:CH2CH2 | B. | H2O的电子式: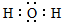 | ||
| C. | 葡萄糖的分子式:C12H22O11 | D. | 14C的原子结构示意图: |
查看答案和解析>>
科目: 来源: 题型:实验题
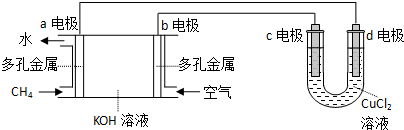
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com