
科目: 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | Na与水反应产生H2:Na+H2O═Na++OH-+H2↑ | |
| C. | 大理石与盐酸反应制取CO2:CO32-+2H+═CO2↑+H2O | |
| D. | 稀硫酸中滴加氢氧化钡溶液:SO42-+2H++2OH-+Ba2+═BaSO4↓+2H2O |
查看答案和解析>>
科目: 来源: 题型:推断题
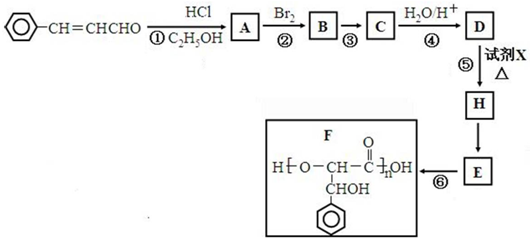
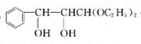 .
. +2Ag(NH3)2OH$\stackrel{△}{→}$
+2Ag(NH3)2OH$\stackrel{△}{→}$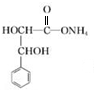 +2Ag↓+3NH3+H2O.
+2Ag↓+3NH3+H2O.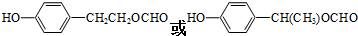 . (任写一种)
. (任写一种)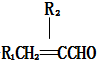
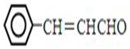 ,设计合成线路(其无机试剂任选),合成线路示意图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=$\stackrel{Br_{2}}{→}$CH2BrH2Br.
,设计合成线路(其无机试剂任选),合成线路示意图示例如下:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=$\stackrel{Br_{2}}{→}$CH2BrH2Br.查看答案和解析>>
科目: 来源: 题型:实验题
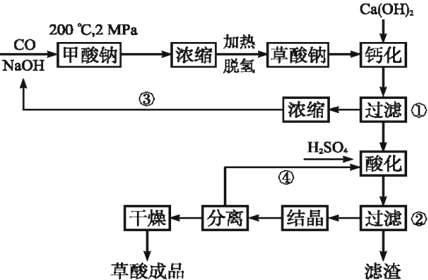
查看答案和解析>>
科目: 来源: 题型:实验题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 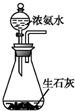 可制取氨气 | |
| B. | 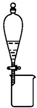 可分离CH3CH2OH和CH3COOC2H5混合液 | |
| C. | 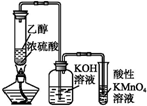 可制取乙烯并验证其易被氧化 | |
| D. | 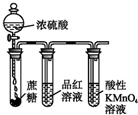 可说明浓硫酸具有脱水性、强氧化性,SO2具有漂白性、还原性 |
查看答案和解析>>
科目: 来源: 题型:实验题
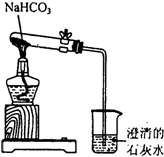 某实验小组的同学为探究碳酸钠、碳酸氢钠的性质,进行了如下实验.请按要求回答下列问题.
某实验小组的同学为探究碳酸钠、碳酸氢钠的性质,进行了如下实验.请按要求回答下列问题.查看答案和解析>>
科目: 来源: 题型:推断题
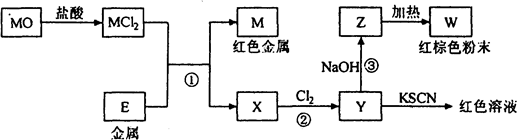
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 漂白粉的主要成分为次氯酸钙 | |
| B. | 实验室可用浓硫酸干燥氨气 | |
| C. | 氯气泄漏时应喷洒盐酸处理毒气 | |
| D. | 实验室可用NaOH溶液处理SO2和HCl等废气 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 乙烯聚合为聚乙烯高分子材料 | B. | 甲烷与氯气制备一氯甲烷 | ||
| C. | 以铜和浓硫酸为原料生产硫酸铜 | D. | 以铜和浓硝酸为原料生产硝酸铜 |
查看答案和解析>>
科目: 来源: 题型:选择题
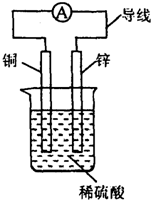
| A. | 铜片是该装置的负极 | |
| B. | 负极反应为Zn-2e-═Zn2+ | |
| C. | 该装置能将电能转化为化学能 | |
| D. | 装置中电流计指针发生偏转,电子由铜片通过导线流向锌 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com