
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,22.4 L二氯甲烷的分子数约为NA个 | |
| B. | 盛有SO2的密闭容器中含有NA个氧原子,则SO2的物质的量为0.5 mol | |
| C. | 17.6 g丙烷中所含的极性共价键为4NA个 | |
| D. | 在过氧化钠与水的反应中,每生成0.1 mol氧气,转移电子的数目为0.4NA |
查看答案和解析>>
科目: 来源: 题型:实验题
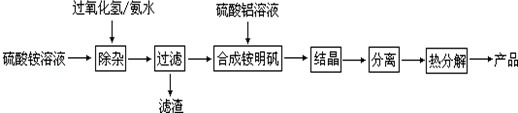
查看答案和解析>>
科目: 来源: 题型:实验题
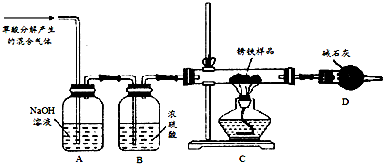
查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 如果人体缺少维生素C,易患夜盲症、干眼症等眼疾 | |
| B. | 维生素C属于脂溶性维生素,主要存在于新鲜水果和蔬菜中 | |
| C. | 维生素C具有较强的还原性,能使酸性高锰酸钾溶液褪色 | |
| D. | 富含维生素C的食物应在高温下烹调,才能充分提高维生素C的功能 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | $\frac{22.4ab}{a{N}_{A}}$ | B. | $\frac{22.4ac}{b{N}_{A}}$ | C. | $\frac{22.4bc}{a{N}_{A}}$ | D. | $\frac{22.4b}{ac{N}_{A}}$ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 22.4L氮气中含NA个氮原子 | |
| B. | 在标准状况下,1mol水的体积约为22.4L | |
| C. | 0.3 mol•L-1Na2SO4溶液中含0.6NA个Na+ | |
| D. | 18 g水中所含的氢原子数目为2NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 未洗涤烧杯和玻璃棒 | B. | 转移溶液前溶液未冷却至室温 | ||
| C. | 容量瓶未干燥 | D. | 定容时俯视 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com