
科目: 来源: 题型:解答题
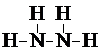 .
.查看答案和解析>>
科目: 来源: 题型:解答题
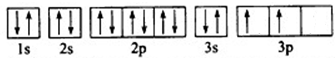
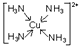 (不考虑空间构型,如有配位键,请标出)
(不考虑空间构型,如有配位键,请标出)查看答案和解析>>
科目: 来源: 题型:解答题
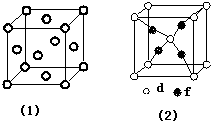 周期表前四周期的元素a、b、c、d、e、f,原子序数依次增大.a是宇宙中最丰富的元素,b的某种核素在考古时用来测定一些文物的年代,d与e同族,用e氧化物漂白的草帽日久又变成黄色;f的最外层只有1个电子,但次外层有18个电子.回答下列问题;
周期表前四周期的元素a、b、c、d、e、f,原子序数依次增大.a是宇宙中最丰富的元素,b的某种核素在考古时用来测定一些文物的年代,d与e同族,用e氧化物漂白的草帽日久又变成黄色;f的最外层只有1个电子,但次外层有18个电子.回答下列问题;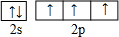 ,f在周期表中的位置是第四周期第IB族
,f在周期表中的位置是第四周期第IB族 .
.查看答案和解析>>
科目: 来源: 题型:解答题
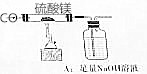 确定反应的化学方程式和制得的MgO的纯度,称量MgSO410.0g,放置于石英管中,按右图连接装置进行试验.试验步骤如下:
确定反应的化学方程式和制得的MgO的纯度,称量MgSO410.0g,放置于石英管中,按右图连接装置进行试验.试验步骤如下:查看答案和解析>>
科目: 来源: 题型:解答题
 (1)“西气东输”中的“气”指天然气,其主要成分的化学式是CH4,
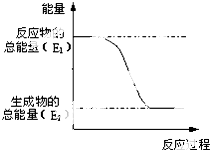
(1)“西气东输”中的“气”指天然气,其主要成分的化学式是CH4,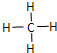 .一定量的该气体燃烧过程的能量变化如图所示,从图中可以读出E1>E2(填“>”或“<”),该反应放出 (填“放出”或“吸收”)能量.
.一定量的该气体燃烧过程的能量变化如图所示,从图中可以读出E1>E2(填“>”或“<”),该反应放出 (填“放出”或“吸收”)能量.查看答案和解析>>
科目: 来源: 题型:解答题
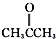 ③CH3CH2Br ④
③CH3CH2Br ④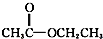 ⑤
⑤
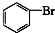 ⑦
⑦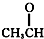 ⑧
⑧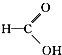 ⑨
⑨ ⑩
⑩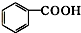
查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com