
科目: 来源: 题型:选择题
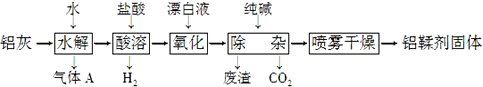
| A. | 气体A能使湿润的红色石蕊试纸变蓝 | |
| B. | “水解”采用90℃而不在室温下进行的原因是加快AlN的水解和使氨气溢出 | |
| C. | “废渣”成分为Al(OH)3和Fe(OH)3 | |
| D. | 采用喷雾干燥而不用蒸发的原因是防止Al(OH)2Cl水解 |
查看答案和解析>>
科目: 来源: 题型:选择题
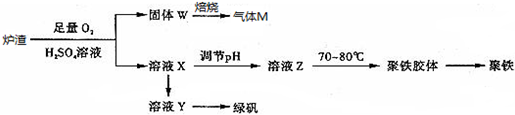
| A. | 炉渣中FeS与硫酸和氧气的反应的离子方程式为:4FeS+3O2+12H+═4Fe3++4S↓+6H2O | |
| B. | 溶液Z的pH影响聚铁中铁的质量分数,若其pH偏小,将导致聚铁中铁的质量分数偏大 | |
| C. | 气体M的成分是SO2,通入双氧水得到硫酸,可循环使用 | |
| D. | 向溶液X中加入过量铁粉,充分反应后过滤得到溶液Y,再经蒸发浓缩、冷却结晶、过滤等步骤得到绿矾 |
查看答案和解析>>
科目: 来源: 题型:实验题
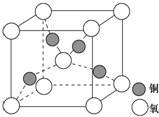 目前半导体生产展开了一场“铜芯片”革命--在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:
目前半导体生产展开了一场“铜芯片”革命--在硅芯片上用铜代替铝布线,古老的金属铜在现代科技应用上取得了突破,用黄铜矿(主要成分为CuFeS2)生产粗铜,其反应原理如下:查看答案和解析>>
科目: 来源: 题型:选择题
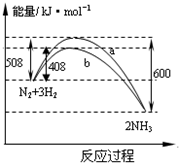
| A. | 该反应的热化学方程式为:$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)?NH3(g)△H=-92kJ•mol-1 | |
| B. | 曲线b表明加入催化剂降低了反应热,加快了反应速率 | |
| C. | 加入催化剂,生成1molNH3的反应热减小50KJ | |
| D. | 不用催化剂,生成1molNH3放出的热量为46KJ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 4个-CH3,能生成4种一氯取代物 | B. | 3个-CH3,能生成3种一氯取代物 | ||
| C. | 3个-CH3,能生成4种一氯取代物 | D. | 2个-CH3,能生成4种一氯取代物 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该反应在发生过程中要吸收能量 | |
| B. | 该反应在发生过程中要放出能量 | |
| C. | 反应后若生成2 mol HCl,则一定会放出2×431 kJ的能量 | |
| D. | 断开1 mol H-H键要吸收的能量与形成1 mol H-Cl键要放出的能量相等 |
查看答案和解析>>
科目: 来源: 题型:选择题
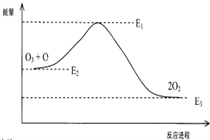
| A. | △H=△H1+△H2 | |
| B. | ClO中含有极性共价键 | |
| C. | 反应O3+O→2O2的△H=E1-E3 | |
| D. | 氯原子改变了该反应的历程,但不影响△H |
查看答案和解析>>
科目: 来源: 题型:填空题

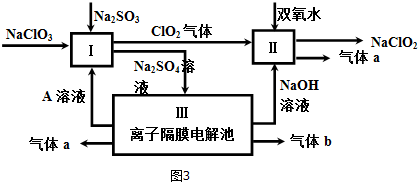
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com