
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Al3+ | B. | Al(OH)3 | C. | AlO2- | D. | Al3+和Al(OH)3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Ba2+和NO3- | B. | Na+和Cl- | C. | Ag+和SO42- | D. | Na+和NO3- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | H+、Na+、SO42-、Cu2+ | B. | Ba2+、Mg2+、Cl-、SO42- | ||
| C. | H+、K+、OH-、NO3- | D. | NO3-、I-、H+、Mg2+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 过氧化钠和水反应 Na2O2+H2O=2Na++2OH-+O2↑ | |
| B. | 金属铝溶于氢氧化钠溶液:Al+2OH-=AlO2-+H2↑ | |
| C. | Ca(ClO)2溶液中通入少量二氧化碳:ClO-+H2O+CO2=HClO+CO32- | |
| D. | 向氯化铝溶液中滴入足量氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1.16 mol•L-1 | B. | 6.8 mol•L-1 | C. | 13.9 mol•L-1 | D. | 20.0 mol•L-1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向3mL1mol/L的碳酸钠溶液中逐滴滴入稀盐酸,起初并无气体生成 | |
| B. | 漂白粉的有效成分是Ca(ClO)2 | |
| C. | 浓硝酸可以盛放在铝制容器中 | |
| D. | 钠元素性质活泼,不可能应用在电光源上 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①③ | B. | ①④⑤ | C. | ②④⑤ | D. | ①⑤ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1.8 g 的NH4+中含有的电子数为NA | |
| B. | 11.2L氯气与钠反应完全转化为氯化钠时得到的电子数为NA | |
| C. | 常温常压下,48gO3含有的氧原子数为NA | |
| D. | 标况下,11.2 L四氯化碳所含的分子数为0.5NA |
查看答案和解析>>
科目: 来源: 题型:实验题
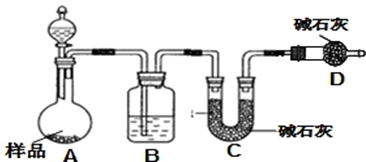
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com