
科目: 来源: 题型:解答题

 .
.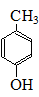 .
.查看答案和解析>>
科目: 来源: 题型:解答题
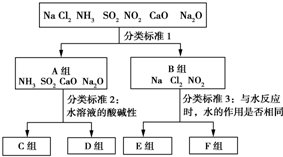
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 沉淀乙一定有BaCO3,可能有BaSO4 | |
| B. | 该溶液A中一定有NO3-、Al3+、SO42-、Cl- | |
| C. | 实验消耗Cu 14.4 g,则生成气体丙为3.36L | |
| D. | 生成的甲、乙、丙气体均为无色的易溶于水气体 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Cl-一定存在,且c(Cl-)≥0.4 mol/L | |
| B. | SO42-、NH4+一定存在,Cl-可能不存在 | |
| C. | CO32-、Al3+一定不存在,K+可能存在 | |
| D. | 至少存在5种离子 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | X可用新制的氢氧化铜检验 | |
| B. | 由Y生成乙酸乙酯的反应属于取代反应 | |
| C. | 反应X→Y中,1molX可生成3molY | |
| D. | 可用碘的四氯化碳溶液检验淀粉是否水解完全 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ③④ | B. | ①③④ | C. | ②③④ | D. | ④⑤ |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:实验题
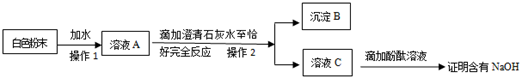
查看答案和解析>>
科目: 来源: 题型:实验题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com