
科目: 来源: 题型:解答题
| 碳 | 氮 | Y | |
| X | 硫 | Z |
查看答案和解析>>
科目: 来源: 题型:解答题
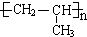 .
.查看答案和解析>>
科目: 来源: 题型:推断题
 R可以被KMnO4的酸性溶液氧化生成
R可以被KMnO4的酸性溶液氧化生成 COOH,但若烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到
COOH,但若烷基R中直接与苯环连接的碳原子上没有C-H键,则不容易被氧化得到 COOH.现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成为
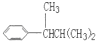
COOH.现有分子式是C11H16的一烷基取代苯,已知它可以被氧化成为 COOH的异构体共有7种,其中的3种是:
COOH的异构体共有7种,其中的3种是: CH2CH2CH2CH2CH3,
CH2CH2CH2CH2CH3,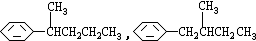
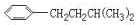 ,
,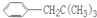 ,
, ,
, .
.查看答案和解析>>
科目: 来源: 题型:填空题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅤⅠA | ⅤⅡA | 0 |
| 1 | A | |||||||
| 2 | B | C | D | E | ||||
| 3 | F | G | H | I | J | K | ||
| 4 | L | M |
查看答案和解析>>
科目: 来源: 题型:填空题
| ⅠA | ⅧA | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | ⑧ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑨ | ||||
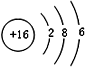 ;
;查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 四联苯(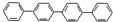 )的一氯代物有4种 )的一氯代物有4种 | |
| B. | 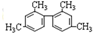 分子中至少有11个碳原子处于同一平面 分子中至少有11个碳原子处于同一平面 | |
| C. | 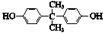 与 与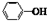 互为同系物 互为同系物 | |
| D. | 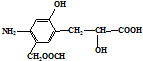 可以发生加成、取代、中和、消去反应 可以发生加成、取代、中和、消去反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
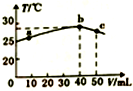
| A. | 25℃时,HA的电离平衡常数Ka约为1.43×10-3 | |
| B. | a→b的过程中,溶液中c(A-)与c(HA)之和始终不变 | |
| C. | b→c的过程中,温度降低的主要原因是溶液中发生了吸热反应 | |
| D. | 等浓度的NaOH和NaA混合溶液中一定存在关系:c(Na+)>c(A-)>c(OH-)>c(H+) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1,3二氯丙烷 | B. | 1,1二氯丙烷 | C. | 1,2二氯丙烷 | D. | 2,2二氯丙烷 |
查看答案和解析>>
科目: 来源: 题型:实验题
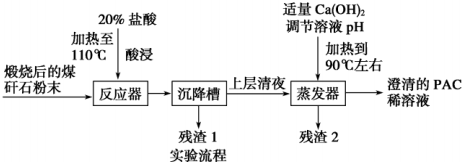
查看答案和解析>>
科目: 来源: 题型:实验题
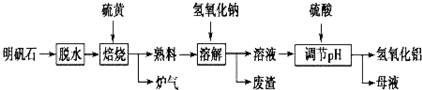
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com