
科目: 来源: 题型:解答题

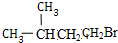 +NaOH$→_{△}^{乙醇}$
+NaOH$→_{△}^{乙醇}$ +NaBr+H2O;
+NaBr+H2O; +HBr$\stackrel{△}{→}$
+HBr$\stackrel{△}{→}$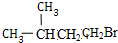 +H2O;
+H2O; ;
; 和
和 ;
;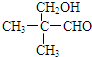 .
.查看答案和解析>>
科目: 来源: 题型:解答题
 已知Q、R、X、Y、Z、W都是周期表中前四周期的元素,它们的核电荷数依次增大,其中Q原子外层电子数是内层电子数的两倍;化合物R2Z的晶体为离子晶体,Z原子核外的M层中有两对成对电子;X元素最外层电子数与最内层电子数相同;Y单质的晶体类型在同周期的单质中没有相同的;W元素所在族有三列,只有两个未成对的电子.请根据以上信息,回答下列问题:(答题时,Q、R、X、Y、Z、W用所对应的元素符号表示)
已知Q、R、X、Y、Z、W都是周期表中前四周期的元素,它们的核电荷数依次增大,其中Q原子外层电子数是内层电子数的两倍;化合物R2Z的晶体为离子晶体,Z原子核外的M层中有两对成对电子;X元素最外层电子数与最内层电子数相同;Y单质的晶体类型在同周期的单质中没有相同的;W元素所在族有三列,只有两个未成对的电子.请根据以上信息,回答下列问题:(答题时,Q、R、X、Y、Z、W用所对应的元素符号表示)查看答案和解析>>
科目: 来源: 题型:解答题
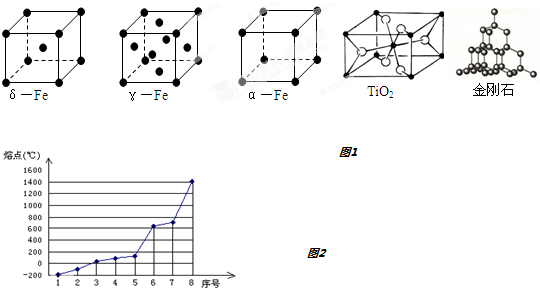
| 共价键 | C-C | O=O | C=O |
| 键能/kJ•mol-1 | a | b | c |
查看答案和解析>>
科目: 来源: 题型:解答题
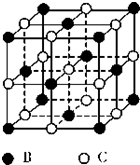 有A、B、C、D、E五种原子序数依次增大的元素(原子序数均不大于30).A的基态原子2p能级有3个单电子;C的核外没有成单电子,B、C两元素形成的化合物晶胞结构如图所示;D的3p能级有1个单电子,且与B所在主族相邻;E元 素在地壳中含量居第四位;则:
有A、B、C、D、E五种原子序数依次增大的元素(原子序数均不大于30).A的基态原子2p能级有3个单电子;C的核外没有成单电子,B、C两元素形成的化合物晶胞结构如图所示;D的3p能级有1个单电子,且与B所在主族相邻;E元 素在地壳中含量居第四位;则:查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 实验事实 | 理论解释 |
| A | 氮原子的第一电离能大于氧原子 | 氮原子2p能级半充满 |
| B | 足球烯(C60)在苯中的溶解度大 | 足球烯是原子晶体 |
| C | 金刚石的熔点低于石墨 | 金刚石是分子晶体,石墨是原子晶体 |
| D | HF的沸点高于HCl | HF的相对分子质量小于HCl |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 46g NO2和N2O4的混合气体中含有的原子个数为3NA | |
| B. | 常温下,4 g CH4含有NA个C-H共价键 | |
| C. | 10 mL质量分数为98%的H2SO4,加水至100 mL,H2SO4的质量分数为9.8% | |
| D. | 25℃时,pH=12的1.0 LNaClO溶液中水电离出的OH-的数目为0.01NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 铝和铜具有良好的导电性,所以电工操作时,可以把铜线和铝线绞接在一起 | |
| B. | 汽车尾气中含有能污染空气的氮的氧化物,原因是汽油燃烧不充分 | |
| C. | 用新制备的Cu(OH)2悬浊液与病人尿液共热,可检验病人尿液中是否含有葡萄糖 | |
| D. | 某雨水样品采集后放置一段时间,pH值由4.68变为4.28,是因为水中溶解了较多的CO2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 硝酸见光易分解,故需保存在棕色瓶中 | |
| B. | Na2CO3、NaAlO2溶液显碱性,故只能用橡胶塞保存 | |
| C. | FeCl2溶液保存时需加入少量铁粉和盐酸 | |
| D. | 少量白磷可保存在煤油中 |
查看答案和解析>>
科目: 来源: 题型:解答题
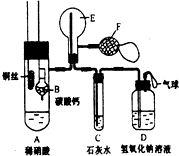 为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球.
为了证明铜与稀硝酸反应产生一氧化氮,某校学生实验小组设计了一个实验,其装置如图所示(加热装置和固定装置均已略去),B为一个用金属丝固定的干燥管,内装块状碳酸钙固体;E为一个空的蒸馏烧瓶;F是用于鼓入空气的双连打气球. 查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 四种元素的原子半径:Z<Y<X<W | |
| B. | 化合物Z2Y与ZW中的化学键类型相同 | |
| C. | X与W两种元素的最简单氢化物间能发生化合反应 | |
| D. | 常温下,X和Y形成的所有化合物均为无色气体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com