
科目: 来源: 题型:实验题
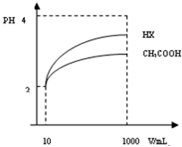 25℃时,部分物质的电离平衡常数如表所示:
25℃时,部分物质的电离平衡常数如表所示:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
查看答案和解析>>
科目: 来源: 题型:解答题
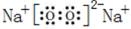 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在4mL0.1mol•L-1的K2Cr2O7溶液中滴加数滴1mol•L-1的NaOH溶液,溶液颜色从橙色变成黄色 | |
| B. | 配制0.1 mol/L的H2SO4溶液时,将量取的浓H2SO4放入容量瓶中加水稀释 | |
| C. | 用干燥且洁净的玻璃棒蘸取NaClO溶液,滴到放在表面皿上的pH试纸上测pH值 | |
| D. | 在用简易量热计测定反应热时,可使用碎泡沫起隔热保温的作用,迅速混合后测出初始温度,用环形玻璃搅拌棒进行搅拌使酸和碱充分反应、准确读取实验时温度计最高温度、并且取2-3 次的实验平均值等措施,以达到良好的实验效果 |
查看答案和解析>>
科目: 来源: 题型:实验题
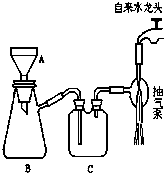 如图所示为减压过滤装置,回答有关问题.
如图所示为减压过滤装置,回答有关问题.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.2 mol•L-1 NH3•H2O溶液与0.1 mol•L-1盐酸等体积混合:c(NH4+)>c(Cl-)>c(OH-)>c(H+) | |
| B. | 0.1 mol•L-1 NaHCO3溶液:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| C. | 向0.2 mol•L-1 NaHCO3溶液中加入等体积的 0.1 mol•L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | 0.1 mol•L-1 Na2CO3溶液:c(HCO3-)+c(H2CO3)=c(OH-)-c(H+) |
查看答案和解析>>
科目: 来源: 题型:解答题
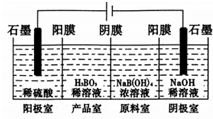
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Fe3+、AlO2-、Cl- | B. | Na+、NH4+、S2- | C. | H+、Cl-、Fe2+ | D. | Mg2+、Ba2+、Br- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | MgO、Al2O3的熔点很高,可作耐高温材料,工业上用热还原法冶炼对应的金属 | |
| B. | 氢氧化钠、碳酸氢钠、氢氧化铝都可用作抗酸药 | |
| C. | 甲醛的水溶液具有杀菌、防腐的作用,可用于海产品保鲜 | |
| D. | 糖类、油脂、蛋白质、维生素、无机盐和水是人体所需的六大营养素 |
查看答案和解析>>
科目: 来源: 题型:推断题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com