
科目: 来源: 题型:解答题
 请回答下列问题:
请回答下列问题:查看答案和解析>>
科目: 来源: 题型:实验题
查看答案和解析>>
科目: 来源: 题型:填空题
 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氯原子的结构示意图: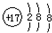 | |
| B. | 作为相对原子质量测定标准的碳核素为${\;}_{6}^{14}$C | |
| C. | 氯化镁的电子式: | |
| D. | HClO的结构式为H-Cl-O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2:3:1 | B. | 1:3:2 | C. | 2:3:3 | D. | 3:2:1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 若反应物总能量大于生成物总能量则反应为放热反应 | |
| B. | 电池工作时将化学能转变成电能 | |
| C. | 绿色植物光合作用过程中太阳能转变成化学能 | |
| D. | 生物质能只能通过含有生物质能的物质的直接燃烧转化成热能从而被利用 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2A(g)+6B(g)?3C(g)+5D(g) | B. | 3A(g)+B(g)?2C(g)+2D(g) | C. | 3A(g)+B(g)?C(g)+D(g) | D. | A(g)+3B(g)?3C(g)+3D(g) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NaOH、Mg(OH)2、Al(OH)3的碱性逐渐增强 | B. | HClO4、HBrO4、HIO4的酸性逐渐减弱 | ||
| C. | I-、Cl-、F-的还原性逐渐减弱 | D. | PH3、H2S、HCl的稳定性逐渐增强 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 单位时间内生成3n molX,同时生成n mol Y | |
| B. | X的生成速率与Z的生成速率相等 | |
| C. | X、Y、Z的浓度不再改变 | |
| D. | X、Y、Z的分子个数比为3:1:2 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com