
科目: 来源: 题型:实验题
| 实验方案 |
| 1.用砂纸打磨后的镁带加适量水加热,再向反应后溶液中滴加酚酞 |
| 2.钠与滴有酚酞试液的冷水反应 |
| 3.镁带与2mol/L的盐酸反应 |
| 4.铝条与2mol/L的盐酸反应 |
| 5.向氯化铝溶液中滴加氢氧化钠溶液至过量 |
| 实验现象 |
| (A) |
| (B)反应不十分强烈,产生气体 |
| (C)剧烈反应,产生气体 |
| (D)生成白色胶状沉淀,然后沉淀消失 |
| (E)产生的气体可在空气中燃烧,溶液变成浅红色 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CO2+H2O=H2CO3和H2CO3=CO2+H2O | |
| B. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑和2H2+O2$\frac{\underline{\;点燃\;}}{\;}$2H2O | |
| C. | 2SO2+O2$\frac{\underline{催化剂}}{△}$2SO3和2SO3$\frac{\underline{催化剂}}{△}$2SO2+O2 | |
| D. | H2+I2$\frac{\underline{\;\;△\;\;}}{\;}$2HI和2HI$\frac{\underline{\;\;△\;\;}}{\;}$H2+I2 |
查看答案和解析>>
科目: 来源: 题型:实验题
| 实验操作 | 实验现象 |
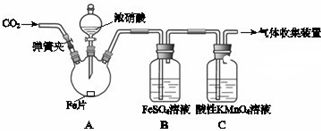
| 打开弹簧夹,通入一段时间CO2,关闭弹簧夹. | |
| 打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞. | 无明显现象. |
| 加热烧瓶,反应开始后停止加热. | ①A中有红棕色气体产生,一段时间后,B中溶液变棕色; C中溶液紫色变浅. ②反应停止后,A中无固体剩余. |
查看答案和解析>>
科目: 来源: 题型:解答题
 ,又知乙与DB2可进行反应,写出相应的化学方程式Na2O2+SO2=Na2SO4.
,又知乙与DB2可进行反应,写出相应的化学方程式Na2O2+SO2=Na2SO4.查看答案和解析>>
科目: 来源: 题型:选择题
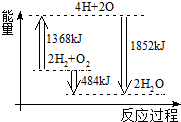
| A. | 拆开2 mol H2(g)和1 mol O2(g)中的化学键成为H、O原子,共放出1368 kJ能量 | |
| B. | 由H、O原子形成2 mol H2O(g),共吸收1852 kJ能量 | |
| C. | 2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(l),共吸收484 kJ能量 | |
| D. | 2 mol H2(g)和1 mol O2(g)反应生成2 mol H2O(g),共放出484 kJ能量 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 氯水、二氧化硫、活性炭的漂白或脱色原理虽然不同,但它们都能使品红或墨迹褪色 | |
| B. | 等物质的量的Cl2和SO2同时与潮湿的红布条作用,红布条立即褪色 | |
| C. | 反应CuSO4+H2S=CuS↓+H2SO4能进行,说明硫化铜既不溶于水,也不溶于稀硫酸 | |
| D. | 经Cl2和SO2漂白的物质,日后都会恢复原来的颜色 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 单质易溶于水 | B. | 最高价氧化物对应水化物是酸 | ||
| C. | 单质既有氧化性又有还原性 | D. | 气态氢化物的稳定性较H2S弱 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com