
科目: 来源: 题型:解答题
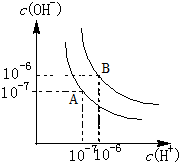 按要求填空:
按要求填空:查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:实验题
查看答案和解析>>
科目: 来源: 题型:填空题
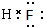 ;
;查看答案和解析>>
科目: 来源: 题型:解答题

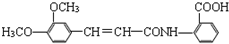 ).
).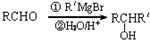
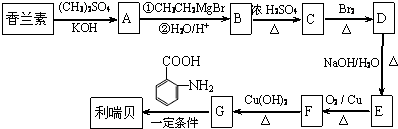
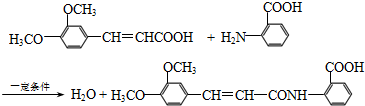
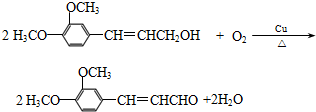
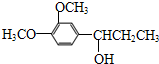 .
.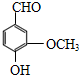 .
.查看答案和解析>>
科目: 来源: 题型:选择题
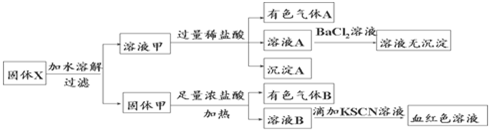
| A. | 溶液甲中一定含有K2SiO3、NaNO2、可能含有KAlO2、K2CO3 一定不含有K2SO3 | |
| B. | 沉淀A为H2SiO3 | |
| C. | 气体A和气体B一定均为纯净物 | |
| D. | 原混合物中一定含有Fe2O3 |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 步骤I可知W中一定存在Fe2O3和Cu | |
| B. | 步骤II可知4.7gW中SiO2的质量为1.5g | |
| C. | 根据步骤I、II可以判断W中一定存在Cu、Fe2O3、SiO2 | |
| D. | 根据上述步骤I、II可以得出m(Fe2O3):m(Cu)=1:1 |
查看答案和解析>>
科目: 来源: 题型:实验题
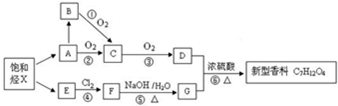
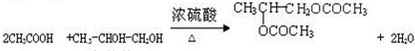 .
.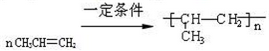 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com