
科目: 来源: 题型:选择题
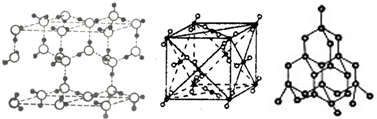
| A. | 冰晶体中只存在分子间作用力和氢键 | |
| B. | 沸点:金刚石>干冰>冰 | |
| C. | 冰晶体中的氧原子和金刚石中的碳原子可形成四面体结构 | |
| D. | 干冰晶体中每个CO2周围等距离且最近的CO2有10 个 |
查看答案和解析>>
科目: 来源: 题型:选择题
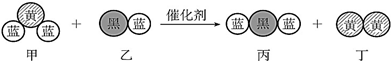 汽车尾气中常常含有CO、NOx等气体,为减轻污染,当代汽车都加装了“三效催化净化器”,可将汽车尾气中的有毒气体处理为无污染的气体,如图为该反应的微观示意图(未配平),其中不同符号的球代表不同种原子.下列说法不正确的是( )
汽车尾气中常常含有CO、NOx等气体,为减轻污染,当代汽车都加装了“三效催化净化器”,可将汽车尾气中的有毒气体处理为无污染的气体,如图为该反应的微观示意图(未配平),其中不同符号的球代表不同种原子.下列说法不正确的是( )| A. | 甲、乙、丙、丁中有3 种非极性分子 | |
| B. | 甲和丁中同种元素化合价不相等 | |
| C. | H2CO3、HNO3的相对强弱与分子中键的极性相关 | |
| D. | N2O5的水化物中不存在氢键 |
查看答案和解析>>
科目: 来源: 题型:选择题
| H2O | H2S | H2Se | H2Te |
| 100℃ | -60.75℃ | -41.5℃ | -1.8℃ |
| A. | 氧族元素氢化物沸点高低与范德华力的大小无关 | |
| B. | 范德华力一定随相对分子质量的增大而减小 | |
| C. | 水分子间可能还存在一种特殊的分子间作用力 | |
| D. | 水分子间存在共价键,加热时较难断裂 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 参加反应的Zn质量一定相等 | B. | 硫酸反应完全,CH3COOH有剩余 | ||
| C. | 两种酸都有剩余 | D. | 参加反应的Zn的质量比为3:4 |
查看答案和解析>>
科目: 来源: 题型:选择题
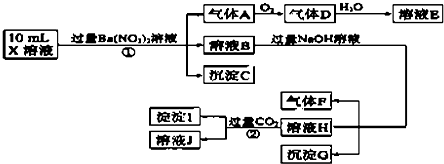
| A. | 由实验①可知,气体A一定是NO,沉淀C一定是BaSO4,原溶液中肯定含有SO32- | |
| B. | 溶液E和气体F不能发生化学反应 | |
| C. | 由实验 ②可知,沉淀I可能是Al(OH)3和BaCO3 | |
| D. | 原溶液中肯定含有Al3+、NH4+、Fe2+、SO42-、Cl-,不能确定是否含有Fe3+ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | W的简单氢化物稳定性比Z的简单氢化物稳定性低 | |
| B. | Y与W形成的化合物YW2的熔点高、硬度大 | |
| C. | W与X形成的两种化合物中阴、阳离子的个数比均为1:2 | |
| D. | Y、R、Z最高价氧化物对应水化物的酸性强弱顺序:Z>R>Y |
查看答案和解析>>
科目: 来源: 题型:解答题
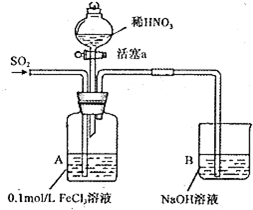
| 实验 序号 | 实验操作 | 实验现象 |
| I | 向A装置中通入一段时间的SO2气体. | A中黄色溶液最终变为浅绿色. |
| II | 取出少量A装置中的溶液,先加入 KSCN溶液,再加入BaCl2溶液. | 加人KSCN溶液后溶液不变色;再加入BaCl2溶液产生白色沉淀. |
| III | 打开活塞a,将过量稀HNO3加入装置A 中,关闭活塞a. | A中浅绿色溶液最终变为黄色. |
| V | 取出少量A装置中的溶液,加入KSCN 溶液. | 溶液变为红色. |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 反应后SO2有剩余 | |
| B. | 溶液还可吸收SO2 | |
| C. | 溶液中除OH-外,只存在一种阴离子 | |
| D. | 溶液中溶质(正盐与酸式盐)的物质的量之比为2:1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com