
科目: 来源: 题型:选择题
| A. | 冷的浓硫酸和浓硝酸都不可以用铝、铁的容器盛装 | |
| B. | 所有铵盐都易溶于水,所有铵盐中的氮均呈-3价 | |
| C. | 由于铵盐易和碱反应生成氨气,所以在实验室中一般用NH4Cl和NaOH的混合物制取氨气 | |
| D. | 金和铂不溶于浓硫酸和浓硝酸,但能溶于王水 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 用浓硫酸做干燥剂 | |
| B. | 将火柴梗插入浓硫酸中,火柴梗很快变黑 | |
| C. | 铜与浓硫酸加热时发生反应 | |
| D. | 锌与稀硫酸发生置换反应制取氢气 |
查看答案和解析>>
科目: 来源: 题型:多选题
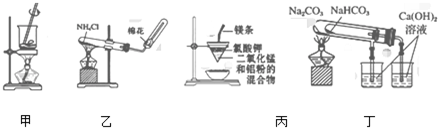
| A. | 用甲图装置灼烧海带成海带灰 | |
| B. | 用乙图装置实验室制氨气 | |
| C. | 用丙图装置可制得金属锰 | |
| D. | 用丁图装置验证NaHCO3和Na2CO3的稳定性 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 对于相同pH的弱酸HX和HY(前者的Ka较小),加水稀释后pH值仍相同,则前者酸中稀释的倍数更大 | |
| B. | 在CH3COOH和CH3COONa浓度均为0.1mol/L的体系中,外加少量强碱时,溶液的PH值发生较大变化 | |
| C. | 在Na2HPO4水溶液中存在关系式:c(H3PO4)+c(H2PO4-)+c(HPO42-)+c(PO43-)═c(Na+) | |
| D. | 沉淀溶解平衡BaSO4═Ba2++SO42- 的沉淀溶解平衡常数为1.1×10-10,说明难溶盐BaSO4是弱电解质 |
查看答案和解析>>
科目: 来源: 题型:解答题
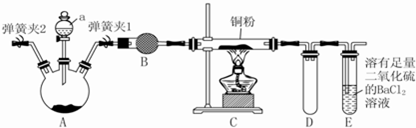
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,11.2L的戊烷所含的分子数大于0.5NA | |
| B. | 28g乙烯所含共用电子对数目为4NA | |
| C. | 标准状况下,11.2 L二氯甲烷所含分子数为0.5NA | |
| D. | 现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为2NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | υ(A)=0.5 mol/(L•s) | B. | υ(B)=0.3 mol/(L•s) | C. | υ(C)=12 mol/(L•min) | D. | υ(D)=6 mol/(L•min) |
查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com