
科目: 来源:2017届河南省高三上第二次月考化学试卷(解析版) 题型:填空题
【选做题——物质结构与性质】
早期发现的一种天然二十面体准晶颗粒由 Al、Cu、Fe 三种金属元素组成,回答下列问题:
(1)准晶是一种无平移周期序,但有严格准周期位置序的独特晶体,可通过___________方法区分晶体、准晶体和非晶体。
(2)基态Fe原子有个___________个未成对电子。Fe3+的电子排布式为_____________ 。
(3)新制备的Cu(OH)2可将乙醛(CH3CHO)氧化为乙酸,而自身还原成Cu2O。乙醛中碳原子的杂化轨道类型为__________,1 mol乙醛分子中含有的σ键的数目为______________。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有___________个铜原子。锗也是一种半导体材料,Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键,从原子结构角度分析,原因是_______________________。
(4)如图是金属Ca和D所形成的某种合金的晶胞结构示意图

镧镍合金与上述合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力。已知镧镍合金LaNin晶胞体积为9.0×10-23 cm3,储氢后形成LaNinH4.5合金(氢进入晶胞空隙,体积不变),则LaNin中n=_____________(填数值);氢在合金中的密度为_____________。
查看答案和解析>>
科目: 来源:2017届河南省高三上第二次月考化学试卷(解析版) 题型:推断题
【选做题——有机化学基础】
四苯基乙烯(TPE)及其衍生物具有诱导发光特性,在光电材料等领域应用前景广阔。以下是TPE的两条合成路线(部分试剂和反应条件省略):

(1)A的名称是________;试剂Y为____________。
(2)B→C、F→D的反应类型依次是_____________、_____________;B中官能团的名称是________,D中官能团的名称是____________。
(3)已知E的化学式为C13H11Br,E→F的化学方程式是_________________。F→D的化学方程式是________________________。
(4)W是D的同分异构体,具有下列结构特征:①属于萘( )的一元取代物;②存在羟甲基( -CH2OH)。写出W所有可能的结构简式:______________________。
)的一元取代物;②存在羟甲基( -CH2OH)。写出W所有可能的结构简式:______________________。
(5)下列说法正确的是___________。
a.B的酸性比苯酚强 b.D不能发生还原反应
c.E含有3种不同化学环境的氢 d.TPE既属于芳香烃也属于烯烃
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 铁是黑色金属,所以断口是黑色的 | B. | 铁是第ⅧB族元素,也是过渡元素 | ||
| C. | 在自然界中无游离态的铁存在 | D. | 自然界里含铁的矿物质叫铁矿石 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 25℃时,对于pH相同的弱碱ROH和MOH(前者的电离平衡常数Kb较小),加水稀释后溶液的pH仍相同,则后者稀释的倍数更大 | |
| B. | 25℃时,0.1mol•L-1的HA溶液中$\frac{c(O{H}^{-})}{c({H}^{+})}$=1×10-8,则该溶液中由水电离出的c(H+)=1×10-3mol•L-1 | |
| C. | 25℃时,等物质的量浓度、等体积的NH4HSO4溶液和NaOH溶液混合:c(Na+)=c(SO${\;}_{4}^{2-}$)>c(NH${\;}_{4}^{+}$)>c(H+)>c(OH-) | |
| D. | 25℃时,沉淀溶解平衡:BaSO4(s)?Ba2+(aq)+SO${\;}_{4}^{2-}$(aq)的Ksp为1.1×10-10,说明BaSO4是弱电解质 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 24gMg在22.4LO2中恰好燃烧完全 | |
| B. | 标准状况下,5.6LCO2气体中含有的氧原子数为0.5NA | |
| C. | 在烧杯中1molFe与含2mol氯化氢的浓盐酸恰好反应 | |
| D. | 44.8LNH3所含分子数为2NA |
查看答案和解析>>
科目: 来源: 题型:实验题
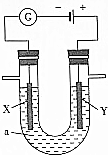 电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
电解原理在化学工业中有广泛的应用.如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 胶体比溶液更稳定 | |
| B. | 从外观一定能区别溶液和胶体 | |
| C. | 用渗析的方法净化胶体时,使用的半透膜只能让离子、小分子通过 | |
| D. | 淀粉溶液不是胶体 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 向某溶液中加入稀盐酸,产生的气体通入澄清石灰水,石灰水变浑浊,该溶液一定含有碳酸根离子 | |
| B. | 配制一定物质的量浓度的硫酸溶液时,用量筒量取一定体积的浓硫酸倒入烧杯后,再用蒸馏水洗涤量筒2~3次,并将洗涤液一并倒入烧杯中稀释 | |
| C. | 称量氢氧化钠固体的质量时,将称量物放在烧杯中,并置于托盘天平的左盘,砝码放在托盘天平的右盘 | |
| D. | 向某溶液中滴加NaOH溶液,溶液中出现蓝色沉淀,该溶液中一定含Cu2+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com