
科目: 来源: 题型:选择题
| A. | 氢氧化镁中滴加盐酸:H++OH-═H2O | |
| B. | 碳酸氢钙溶液与稀硝酸反应:Ca(HCO3)2+2H+=Ca2++CO2↑+H2O | |
| C. | 金属铝溶于氢氧化钠溶液:2Al+6OH-═2AlO2-+3H2↑ | |
| D. | 用FeCl3溶液腐蚀铜电路板:2Fe3++Cu═2Fe2++Cu2+ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 浓度均为0.1 mol•L-1的NaF、CH3COONa溶液相比较,CH3COONa溶液碱性较强 | |
| B. | 0.1 mol•L-1 CH3COOH溶液,加水稀释过程中,所有离子浓度均减小 | |
| C. | NaF溶液中只含有Na+、F-、H+、OH-、H2O五种微粒 | |
| D. | NaF溶液中加入少量NaOH固体,溶液中c(F-)变小 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ③④ | B. | ③⑤ | C. | ①③④ | D. | ①②③ |
查看答案和解析>>
科目: 来源: 题型:解答题
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
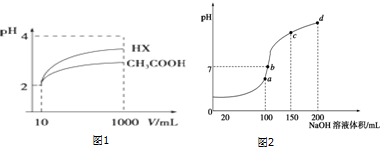
查看答案和解析>>
科目: 来源: 题型:选择题
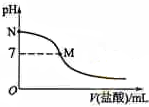 298K时,在20.0mL 0.10mol•L-1氨水中滴入0.10mol•L-的盐酸,溶液的pH与所加盐酸的体积关系如图所示.已知0.10mol•L-1氨水的电离度为1.32%,下列有关叙述正确的是( )
298K时,在20.0mL 0.10mol•L-1氨水中滴入0.10mol•L-的盐酸,溶液的pH与所加盐酸的体积关系如图所示.已知0.10mol•L-1氨水的电离度为1.32%,下列有关叙述正确的是( )| A. | 该滴定过程应该选择石蕊作为指示剂 | |
| B. | M点对应的盐酸体积为20.0 mL | |
| C. | M点处的溶液中c(NH4+)=c(Cl-)=c(H+)=c(OH-) | |
| D. | N点处的溶液中pH<12 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 降低温度可加快该反应速率 | |
| B. | 加入合适的催化剂可提高H2O2转化率 | |
| C. | 达到平衡时,v(正)=v(逆)=0 | |
| D. | 达到平衡时,v正(CH3COOH)=v逆(H2O2) |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 原子半径C>D>A>B | B. | 离子半径D>C>B>A | ||
| C. | 原子序数b>a>c>d | D. | 单质的还原性A>B>C>D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com