
科目: 来源: 题型:解答题
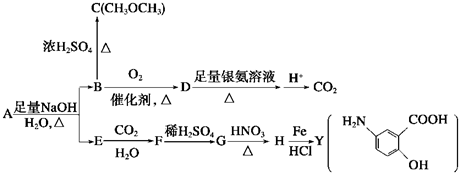
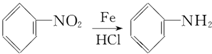
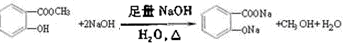 .
.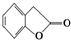 和
和 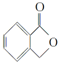 ,鉴别I和J的试剂为FeCl3或浓溴水.
,鉴别I和J的试剂为FeCl3或浓溴水.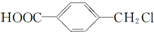 制得,写出K在浓硫酸作用下生成的聚合物的结构简式:
制得,写出K在浓硫酸作用下生成的聚合物的结构简式: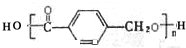 .
.查看答案和解析>>
科目: 来源: 题型:解答题
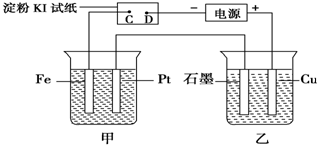
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 该条件下32g S(s)完全燃烧放出的热量为297.23kJ | |
| B. | 反应S(g)+O2(g)═SO2(g)的△H大于-297.3kJ•mol-1 | |
| C. | 反应S(g)+O2(g)═SO2(g)的△H小于-297.3kJ•mol-1 | |
| D. | 形成1 mol SO2(g)中的化学键所释放的总能量大于断裂1 mol S(s)和1mol O2(g)中的化学键所吸收 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
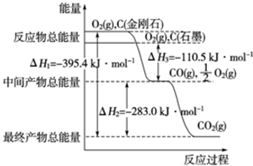 金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示.
金刚石和石墨均为碳的同素异形体,它们燃烧氧气不足时生成一氧化碳,充分燃烧生成二氧化碳,反应中放出的热量如图所示.查看答案和解析>>
科目: 来源: 题型:选择题
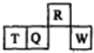 短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )
短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等.下列判断不正确的是( )| A. | 最简单气态氢化物的热稳定性:R>Q | |
| B. | 最高价氧化物对应水化物的酸性:Q<W | |
| C. | 原子半径:T>Q>R | |
| D. | 含T的盐溶液一定能与碱反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 已知2H2(g)+O2(g)=2H2O(l)△H=-483.6 kJ•mol-1,则氢气的燃烧热为483.6 kJ•mol-1 | |
| B. | 已知C(石墨,s)=C(金刚石,s)△H>0,则金刚石比石墨稳定 | |
| C. | 已知2C(s)+2O2(g)=2CO2(g)△H1 2C(s)+O2(g)=2CO(g)△H2 则△H1<△H2 | |
| D. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ•mol-1,若将含0.5 mol H2SO4的浓溶液与含1 mol NaOH的溶液混合,放出的热量等于57.3 kJ |
查看答案和解析>>
科目: 来源: 题型:解答题
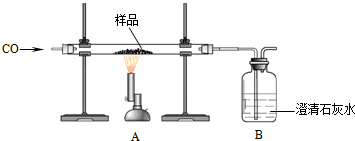
| 样品质量 | 装置A中玻璃管和固体的总质量 | 装置B的质量 |
| 2.50g | 反应前55.56g | 反应前281.00g |
| 反应后55.08g | 反应后281.25g |
查看答案和解析>>
科目: 来源: 题型:实验题
| 实验过程 | 实验现象 |
| 实验1:分别将①、②、③取样于三支试管中,再分别加入溶液④ | ①②无明显变化,③有气泡产生 |
| 实验2:分别将②、③、④取样于三支试管中,再分别加入溶液① | ③、④无明显变化,②溶液变红 |
| 实验3:分别向实验2的三支试管中,继续滴加入足量溶液④ | ④无明显变化,②溶液变红变为无色,③中先无明显现象,之后有气泡产生 |
查看答案和解析>>
科目: 来源: 题型:选择题
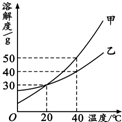
| A. | 20℃时,甲溶液中溶质的质量分数一定等于乙溶液中溶质的质量分数 | |
| B. | 40℃时,分别在100 g水中加入40 g甲、乙,所得溶液溶质的质量分数相等 | |
| C. | 40℃时,分别在100 g水中加入30 g甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液 | |
| D. | 20℃时,分别在100 g水中加入40 g甲、乙,加热到40℃时,乙溶液为饱和溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com