
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:推断题
查看答案和解析>>
科目: 来源: 题型:解答题
 图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 容量瓶事先没有烘干 | B. | 定容时观察液面俯视 | ||
| C. | 定容时观察液面仰视 | D. | 定容后,摇匀时有少量液体流出 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | C8H18(l)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(g)△H=-48.40 kJ•mol-1 | |
| B. | C8H18(l)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(l)△H=-5518 kJ•mol-1 | |
| C. | C8H18(l)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(l)△H=+5518 kJ•mol-1 | |
| D. | C8H18(l)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(l)△H=-48.40 kJ•mol-1 |
查看答案和解析>>
科目: 来源: 题型:解答题
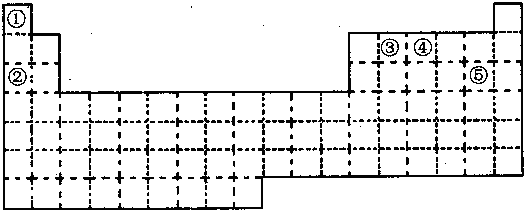
查看答案和解析>>
科目: 来源: 题型:解答题
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(10-10m) | 0.74 | 1.60 | 1.52 | 1.10 | 0.99 | 1.86 | 0.75 | 0.82 |
| 最高或最低化合价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| -2 | -3 | -1 | -3 |
查看答案和解析>>
科目: 来源: 题型:多选题
| 选项 | 需要区分的物质 | 实验方法 | |
| A | 磷酸钙和氯化铵 | 溶于水 | 与熟石灰混合研磨 |
| B | 氢氧化钠固体和熟石灰 | 将两种固体溶于水 | 溶于水,向所得溶液中分别吹入CO2气体 |
| C | 硫酸钾和碳酸钾 | 加硝酸钡溶液 | 加水溶解 |
| D | 硬水和软水 | 肥皂水 | 加热、煮沸 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com