
科目: 来源: 题型:选择题
| A. | 常温下,1LPH=0的硫酸溶液中,H+数为NA | |
| B. | 0.5mol 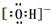 中含有的电子数为4.5NA 中含有的电子数为4.5NA | |
| C. | 7.8gNa2S与Na2O2的混合物中含有的阴离子数目为0.1NA | |
| D. | 0.1mol14N18O与3.1g13C18O的中子数均为1.7NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 由不同的原子形成的纯净物一定属于化合物 | |
| B. | 一种酸性氧化物只能水化生成一种含氧酸 | |
| C. | 铜、苛性钠都属于金属单质 | |
| D. | NaHCO3、BaSO4都属于强电解质 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 卫星上的太阳能电池工作 | |
| B. | 向氢氧化铁胶体中加入稀硫酸产生红褐色沉淀 | |
| C. | 向鸡蛋清中加入饱和硫酸铵溶液,产生白色沉淀 | |
| D. | 向盛有红墨水的试管中加入活性炭,振荡,红色褪去 |
查看答案和解析>>
科目: 来源: 题型:选择题
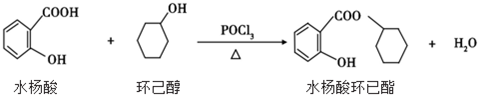
| A. | 水杨酸的核磁共振氢谱有 4 个吸收峰 | |
| B. | 水杨酸、环已醇和水杨酸环已酯都能与 FeCl3 溶液发生显色反应 | |
| C. | 1mol 水杨酸跟浓溴水反应时,最多消耗 2molBr2 | |
| D. | 1mol 水杨酸环已酯在 NaOH 溶液中水解时,最多消耗 3molNaOH |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 一定条件下,C12 可在甲苯的苯环或侧链上发生取代反应 | |
| B. | 乙二酸可与高锰酸钾溶液发生反应 | |
| C. | 乙醇和乙烯的混合物 lmol,完全燃烧消耗 3molO2 | |
| D. | 光照下 2,2-二甲基丁烷与 Br2 反应,其一溴取代物只有 2 种 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 苯酚能跟 NaOH 溶液反应,乙醇不能与 NaOH 溶液反应 | |
| B. | 乙烯能发生加成反应,乙烷不能发生加成反应 | |
| C. | 甲苯能使酸性高锰酸钾溶液褪色,苯不能使酸性高锰酸钾溶液褪色 | |
| D. | 苯与硝酸在加热时发生取代反应,甲苯与硝酸在常温下就能发生取代反应 |
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验序号 | 试剂 | 现象 |
| I | 饱和Ag2SO4溶液 | 产生白色沉淀 |
| II | 0.2mol•L-1CuCl2溶液 | 溶液变绿,继续滴加产生棕黄色沉淀 |
| III | 0.1mol•L-1Al2(SO4)3溶液 | 开始无明显变化,继续滴加产生白色沉淀 |
查看答案和解析>>
科目: 来源: 题型:解答题
 工业上制取氯酸钾的主要步骤为:
工业上制取氯酸钾的主要步骤为: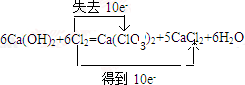 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com