
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. |  | B. |  | C. |  | D. |  |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 液氯是纯净物,氯水是电解质,漂白粉是混合物 | |
| B. | 氯气可用作消毒剂和漂白剂,是因为氯分子具有强氧化性 | |
| C. | 随着化合价的升高,氯的含氧酸酸性和氧化性均逐渐增强 | |
| D. | 不能用pH试纸测定氯水的pH |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 原子、分子、离子都可以构成物质 | |
| B. | 由同种元素构成的物质是纯净物 | |
| C. | 盐酸与氢氧化钠反应一定是复分解反应 | |
| D. | 置换反应中一定有单质生成 |
查看答案和解析>>
科目: 来源: 题型:推断题
 海底热液研究处于当今科研的前沿.海底热液活动区域“黑烟囱”的周围常存在FeS、黄铜矿及锌矿等矿物.
海底热液研究处于当今科研的前沿.海底热液活动区域“黑烟囱”的周围常存在FeS、黄铜矿及锌矿等矿物.| 电离能/kJ•mol-1 | I1 | I2 |
| 铜 | 746 | 1958 |
| 锌 | 906 | 1733 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,1L液态水中含有的H+数目为10-7 NA | |
| B. | 标准状况下,2.24 L D2O中含有的电子数为NA | |
| C. | 3.4g H2O2中含有的共用电子对数为0.1 NA | |
| D. | 1mol碳烯(:CH2)中含有的电子数为8NA |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | Mg和Zn | B. | Zn和Fe、C | C. | Cu和Fe | D. | Zn和Cu |
查看答案和解析>>
科目: 来源: 题型:解答题

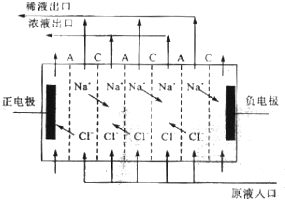
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Al具有良好延展性和抗腐蚀性,可制成铝箔包装物品 | |
| B. | 二氧化硅有良好的导电性,是制造光导纤维的主要材料 | |
| C. | 药皂中加入少量苯酚,可以起到杀菌消毒的作用 | |
| D. | 碳酸钠溶液显碱性,可用热的纯碱溶液除去金属器件表面的油污 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com