
科目: 来源: 题型:选择题
| A. | 通过电解熔融CD3可以制备C单质 | |
| B. | A和B可以形成BA3、B2A4等酸性化合物 | |
| C. | C的氢氧化物可以溶于B或D的最高价氧化物的水化物 | |
| D. | BA4BO3中只存在非金属元素,只存在共价键 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温下干燥氯气与铁不反应,可以用钢瓶储存氯水 | |
| B. | 二氧化硫具有漂白、杀菌性能,可在食品生产中大量使用 | |
| C. | 浓硫酸具有吸水性,可以用来干燥氨气 | |
| D. | 次氯酸钠具有强氧化性,可用于配制消毒液 |
查看答案和解析>>
科目: 来源: 题型:推断题

查看答案和解析>>
科目: 来源: 题型:选择题
 )的缩写代号为PMMA,俗称有机玻璃.下列说法中错误的是( )
)的缩写代号为PMMA,俗称有机玻璃.下列说法中错误的是( )| A. | 聚甲基丙烯酸甲酯属于有机高分子合成材料 | |
| B. | 聚甲基丙烯酸甲酯的分子式可表示为(C5H8O2)n | |
| C. | 合成PMMA的单体是甲基丙烯酸和甲醇 | |
| D. | 甲基丙烯酸甲酯中碳原子可能都处于同一平面 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | SO2具有氧化性,可用于漂白纸浆 | |
| B. | CO具有还原性,可用于冶炼铁等金属 | |
| C. | SiO2熔点高,可用作光导纤维 | |
| D. | Al2O3具有两性,可用作耐高温材料 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 含有0.6mol Ca2+ | B. | 含有0.3mol Cl- | ||
| C. | n(Na+):n(OH-)=1:5 | D. | 所含元素中钙元素的质量很大 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:推断题
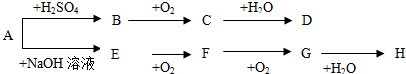
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com