
科目: 来源: 题型:选择题
| A. | HClO的结构式:H-O-Cl | B. | H2O2的电子式: | ||
| C. | 质量数为14碳原子表示方法:14C | D. | 14C的原子结构示意图: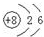 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 离子化合物中一定含有离子键 | |
| B. | 有机聚合高分子中只含有单键 | |
| C. | 乙醇、乙醛和乙酸互为同分异构体 | |
| D. | 纤维素属于天然高分子化合物,分子中含有碳氢两种元素 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 18g D2O所含电子数目为10NA | |
| B. | 实验室用含2molHCl的浓盐酸在加热下与足量的MnO2反应,转移的电子数为NA | |
| C. | 由CO2和O2组成的混合物中共有NA个分子,其中的氧原子数为4NA | |
| D. | 标准状况下,22.4 L氦气与18g水所含分子数均为NA |
查看答案和解析>>
科目: 来源: 题型:选择题
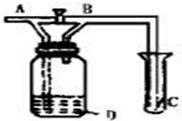 如图所示,A处通入Cl2,关闭B阀时,C处的红布看不到明显现象,当打开B阀后,C处红布条逐渐褪色,则D中装的是( )
如图所示,A处通入Cl2,关闭B阀时,C处的红布看不到明显现象,当打开B阀后,C处红布条逐渐褪色,则D中装的是( )| A. | KNO3溶液 | B. | NaOH溶液 | C. | 水 | D. | 饱和NaCl溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 150 mL 1 mol•L-1NaCl溶液 | B. | 150 mL 3 mol•L-1KCl溶液 | ||
| C. | 75 mL 1.5 mol•L-1FeCl3溶液 | D. | 50 mL 3 mol•L-1MgCl2溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1L 1mo/L的FeCl3溶液中含有的Fe3+为1NA | |
| B. | 标准状况下,22.4L空气含有NA个单质分子 | |
| C. | 1mol铜与足量硫反应,转移的电子总数为NA | |
| D. | 18g D2O(重水)中所含电子个数为10 NA |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 弱酸酸式盐 NaHB 在水溶液中水解:HB-+H2O?H3O++B2- | |
| B. | 工业上电解饱和食盐水:C1-+2H2O$\frac{\underline{\;通电\;}}{\;}$H2↑+Cl2↑+OH- | |
| C. | AlCl3溶液与小苏打溶液混合:Al3++3HCO3-═Al(OH)3↓+3CO2↑ | |
| D. | FeBr2溶液中通入过量 Cl2:2Fe2++2Br-+2Cl2═2Fe3++Br2+4Cl- |
查看答案和解析>>
科目: 来源: 题型:实验题
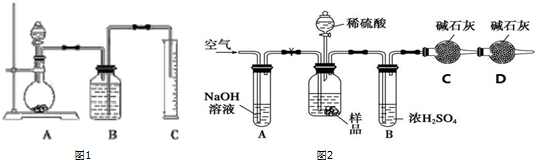
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | ZY、ZW 的水溶液都显酸性 | |
| B. | 原子半径大小:W>R>X,离子半径大小:Z+>R2->W->Y- | |
| C. | W 的氢化物水溶液的酸性比 R 的氢化物水溶液的酸性强,可证明非金属性:W>R | |
| D. | Z、X 两种元素可形成的 Z2X、Z2X2等多种离子化合物 |
查看答案和解析>>
科目: 来源: 题型:选择题
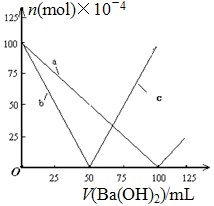 烧杯中盛有 100mL 0.1mol/L 的 NaHSO4溶液,向其中逐滴滴加 0.1mol/L 的 Ba(OH)2溶液,烧杯中某些物质(或微粒)的物质的量的变化曲线如图.下列说法正确的是( )
烧杯中盛有 100mL 0.1mol/L 的 NaHSO4溶液,向其中逐滴滴加 0.1mol/L 的 Ba(OH)2溶液,烧杯中某些物质(或微粒)的物质的量的变化曲线如图.下列说法正确的是( )| A. | 曲线 a 表示 Ba2+的物质的量的变化 | |
| B. | 曲线 c 表示 OH-的物质的量的变化 | |
| C. | 加入 Ba(OH)2溶液 50mL 时反应的离子方程式为:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 加入 Ba(OH)2溶液大于 50mL 后,反应的离子方程式为:OH-+H+═H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com