
科目: 来源: 题型:选择题
| A. | 11% | B. | 19% | C. | 40% | D. | 50% |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②③④ | B. | ②③⑤⑥ | C. | ①③④⑤ | D. | ②③④⑤ |
查看答案和解析>>
科目: 来源: 题型:选择题
| 选项 | 现象 | 解释 |
| A | Cl2在H2中点燃,瓶口有白雾 | 生成HCl极易溶于水 |
| B | 饱和Na2CO3溶液中通入CO2析出白色晶体 | 生成NaHCO3溶解度小析出 |
| C | 常温下将铝片放入浓硝酸中无明显变化 | Al和浓硝酸不反应 |
| D | SO2通入溴水,溴水褪色 | SO2具有还原性. |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | HF可以用于刻蚀玻璃 | |
| B. | 用小苏打(NaHCO3)发酵面团制作馒头 | |
| C. | SO2具有漂白性,可用于漂白纸浆,也可以大量用于漂白食品 | |
| D. | 纯碱用于生产普通玻璃,也可用纯碱溶液来除去物品表面的油污 |
查看答案和解析>>
科目: 来源: 题型:填空题
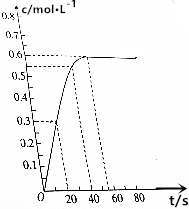 298K时,在2L的恒容密闭容器中,发生可逆反应:2NO2(g)?N2O4(g).N2O4的物质的量浓度随时间的变化如图.达到平衡时N2O4的浓度为NO2的2倍.
298K时,在2L的恒容密闭容器中,发生可逆反应:2NO2(g)?N2O4(g).N2O4的物质的量浓度随时间的变化如图.达到平衡时N2O4的浓度为NO2的2倍.查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
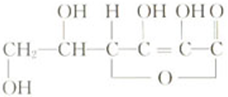 维生素C的结构式如下,
维生素C的结构式如下,查看答案和解析>>
科目: 来源: 题型:推断题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com