
科目: 来源: 题型:推断题


查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 过量的SO2通入NaOH溶液中:SO2+2OH-═SO32-+H2O | |
| B. | 向Al2(SO4)3溶液中加入过量氨水:Al3++3NH3•H2O=Al(OH)3↓+3NH4+ | |
| C. | 过量NaOH滴入NH4HCO3稀溶液中:NH4++OH-═NH3•H2O | |
| D. | 铜片加入稀HNO3中:Cu+2NO3-+4H+═Cu2++2NO2↑+2H2O |
查看答案和解析>>
科目: 来源: 题型:推断题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:推断题
| 元素 | 结构或性质信息 |
| X | 原子的L层上s电子数等于p电子数. |
| Y | 原子核外的L层有3个未成对电子. |
| Z | 在元素周期表的各元素中电负性仅小于氟. |
| M | 单质常温、常压下是气体,原子的M层上有1个未成对的p电子. |
| R | 第四周期过渡元素,其价电子层各能级处于半充满状态 |
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 0.1mol | B. | 0.2mol | C. | 0.15mol | D. | 0.22mol |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 增重30% | B. | 一定增加 | C. | 可能不变 | D. | 减轻30% |
查看答案和解析>>
科目: 来源: 题型:推断题
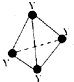 已知X的电负性在同主族元素中最大,其基态原子最外电子层的p轨道呈半充满状态.回答下列问题:
已知X的电负性在同主族元素中最大,其基态原子最外电子层的p轨道呈半充满状态.回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com