
科目: 来源: 题型:选择题
| A. | 稀盐酸可除去烧瓶内残留的MnO2 | B. | 可用磨口玻璃瓶保存NaOH溶液 | ||
| C. | 稀硝酸可除去试管内壁的银镜 | D. | 煮沸自来水可除去其中的CaCO3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 通常状况下,1molCCl4含有的分子数为NA个 | |
| B. | 0.5mol/LNH4Cl溶液中NH4+的数目小于0.2NA个 | |
| C. | 16.0gCuS和CuO的混合物中含有的铜原子数为0.3NA | |
| D. | 向FeI2溶液中通过适量氯气,当有1molFe2+被氧化时,总共转移电子的数目为NA个 |
查看答案和解析>>
科目: 来源: 题型:选择题
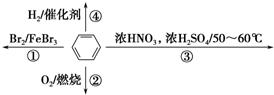
| A. | 反应①为取代反应,有机产物浮在上层 | |
| B. | 反应②为氧化反应,反应现象是火焰明亮并伴有浓烟 | |
| C. | 反应③为取代反应,只生成一种产物 | |
| D. | 反应④中1 mol苯最多与3 mol H2发生加成反应,因为苯分子含有3个碳碳双键 |
查看答案和解析>>
科目: 来源: 题型:解答题
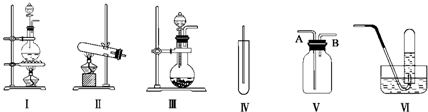
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①② | B. | ①③ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | HCl和NaOH反应的中和热△H=-57.3 kJ/mol,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ/mol | |
| B. | CO(g)的燃烧热△H=-283.0 kJ/mol,则2CO2(g)═2CO(g)+O2(g)反应的△H=+2×283.0 kJ/mol | |
| C. | 需要加热才能发生的反应一定是吸热反应 | |
| D. | 1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 4 v(NH3)=5 v(O2) | B. | 5 v(O2)=6 v(H2O) | C. | 4 v(O2)=5 v(NO) | D. | 2 v(NH3)=3 v(H2O) |
查看答案和解析>>
科目: 来源: 题型:解答题
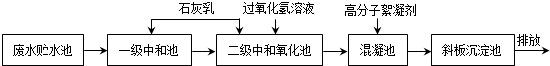
| 离子 | H+ | Cl- | Fe2+ | Fe3+ |
| 浓度(mol/L) | 0.16 | 0.94 | 0.12 |
查看答案和解析>>
科目: 来源: 题型:解答题
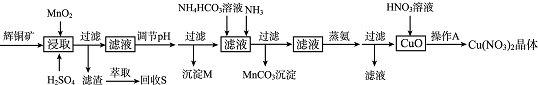
| 离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com