
科目: 来源: 题型:选择题
| A. | c(H+)=c(OH-) | B. | c(OH-)>c(H+) | ||
| C. | c(CH3COOH)>c(CH3COO-) | D. | c(CH3COOH)+c(CH3COO-)=0.02mol/L |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 加热 | |
| B. | 不用稀硫酸,改用质量分数为98%的浓硫酸 | |
| C. | 不用铁片改用镁条 | |
| D. | 不用铁片,改用铁粉 |
查看答案和解析>>
科目: 来源: 题型:解答题
| NaOH 溶液体积/mL | 40.00 | 40.00 | 40.00 |
| 样品质量/g | 7.75 | 15.50 | 23.25 |
| 氨气质量/g | 1.87 | 1.87 | 1.7 |
查看答案和解析>>
科目: 来源: 题型:解答题
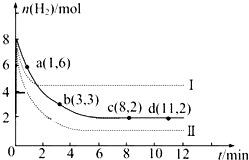 工业上“固定”和利用CO2能有效地减轻“温室”效应,可用CO2生产燃料甲醇:
工业上“固定”和利用CO2能有效地减轻“温室”效应,可用CO2生产燃料甲醇:查看答案和解析>>
科目: 来源: 题型:解答题
 ;液溴的保存通常采取的方法是水封在棕色瓶中,密闭保存.
;液溴的保存通常采取的方法是水封在棕色瓶中,密闭保存.
查看答案和解析>>
科目: 来源: 题型:选择题
 我们能在昏暗的光线下看见物体,离不开视网膜中一种叫“视黄醛”(见甲)的有机化合物,而与视黄醛相似结构的维生素A(见乙)常作为保健药物.则下列有关叙述正确的是( )
我们能在昏暗的光线下看见物体,离不开视网膜中一种叫“视黄醛”(见甲)的有机化合物,而与视黄醛相似结构的维生素A(见乙)常作为保健药物.则下列有关叙述正确的是( )| A. | 视黄醛的分子式为C20H28O | |
| B. | 维生素A分子结构中含有苯环、碳碳双键和羟基 | |
| C. | 维生素A是视黄醛的氧化产物 | |
| D. | 1 mol视黄醛在一定条件下最多能与8 mol H2发生反应 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 2种 | B. | 3种 | C. | 4种 | D. | 5种 |
查看答案和解析>>
科目: 来源: 题型:实验题
查看答案和解析>>
科目: 来源: 题型:填空题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ② | B. | ②③ | C. | ①②③ | D. | ②③④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com