
科目: 来源: 题型:解答题
| 硝酸体积(mL) | 100 | 200 | 300 | 400 |
| 剩余固体(g) | 18.0 | 9.6 | 0 | 0 |
| 放出气体的体积(mL) | 2240 | 4480 | 6720 |
查看答案和解析>>
科目: 来源: 题型:实验题
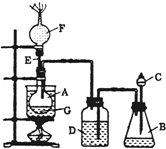 为了证明乙醇分子中含有氧原子,某小组设计了如图装置进行 实验研究.图中烧杯A用作水浴器,锥形瓶B中盛有试剂X,分液漏斗C和广口瓶D中均盛有浓硫酸,E是一根直导管,干燥管F中填满新制的碱石灰,烧瓶G中装有无水乙醇和一些新制白色无水盐粉末Y.打开C处活塞,将浓硫酸慢慢滴入B中与试剂X作用,之后发现D瓶的导管口产生大量气泡,水浴加热G瓶,不久又观察到G瓶中试剂Y变色,F端排出的气体经净化后还能点燃.请回答下列问题:
为了证明乙醇分子中含有氧原子,某小组设计了如图装置进行 实验研究.图中烧杯A用作水浴器,锥形瓶B中盛有试剂X,分液漏斗C和广口瓶D中均盛有浓硫酸,E是一根直导管,干燥管F中填满新制的碱石灰,烧瓶G中装有无水乙醇和一些新制白色无水盐粉末Y.打开C处活塞,将浓硫酸慢慢滴入B中与试剂X作用,之后发现D瓶的导管口产生大量气泡,水浴加热G瓶,不久又观察到G瓶中试剂Y变色,F端排出的气体经净化后还能点燃.请回答下列问题:查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 浓盐酸 | B. | Na2SO4浓溶液 | C. | NaOH浓溶液 | D. | Ba(OH)2浓溶液 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | NaA+H2B→NaHB+HA | B. | 2NaA+H2B→Na2B+2HA | ||
| C. | NaHB+HA→NaA+H2B | D. | Na2B+HA→NaHB+NaA |
查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 金属Na、Mg、A1熔、沸点由高到低 | |
| B. | HC1、HBr、HI的还原性由弱到强 | |
| C. | H+、Li+、H-的半径由小到大 | |
| D. | 同浓度的硫酸钠、乙酸钠、碳酸钠溶液的碱性由强到弱 |
查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:推断题
 、丙
、丙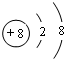 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com