
科目: 来源: 题型:实验题

查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 上述反应属于取代反应 | |
| B. | 对三联苯的一氯取代物有3种 | |
| C. | 1 mol对三联苯在足量的氧气中完全燃烧消耗21.5 mol O2 | |
| D. | 对三联苯分子中至少有16个原子共平面 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将磁性氧化铁溶于盐酸:Fe3O4+8H+═2Fe2++Fe3++4H2O | |
| B. | FeCl3溶液腐蚀铜线路板:Fe3++Cu=Cu2++Fe2+ | |
| C. | 金属铝加入到NaOH溶液中:2Al+2OH-+2H2O═2AlO2-+3H2↑ | |
| D. | 铜与盐酸反应:Cu+2H+═Cu2++H2↑ |
查看答案和解析>>
科目: 来源: 题型:选择题
| 序号 | X | Y | Z | W | 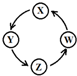 |
| ① | Cu | CuSO4 | Cu(OH)2 | CuO | |
| ② | Na | NaOH | Na2CO3 | NaCl | |
| ③ | Al | AlCl3 | Al(OH)3 | Al2O3 | |
| ④ | Fe | FeCl3 | FeCl2 | Fe(OH)2 |
| A. | ②③ | B. | ①③④ | C. | ①④ | D. | ①②③ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向某溶液中加入氯水,然后加入KSCN溶液,检验该溶液中是否含有Fe2+ | |
| B. | 向偏铝酸钠溶液中通入过量CO2,制备氢氧化铝 | |
| C. | 用金属钠分别与水和乙醇反应,比较水和乙醇分子中羟基氢(-OH)的活泼性 | |
| D. | 用检验Na2CO3和Na2SO4水溶液酸碱性实验,证明碳和硫两元素非金属性的强弱. |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1mol Fe溶于过量稀硝酸,电子转移数为2NA | |
| B. | 标准状况下,2.24L CCl4含有分子的数目为0.1NA | |
| C. | 46g NO2和N2O4混合气体中含有原子总数为3NA | |
| D. | 1L 0.1mol/L的NaHCO3溶液中,HCO3-、CO32-离子数之和为0.1NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 光导纤维在信息领域应用越来越广泛,其主要成分是硅单质 | |
| B. | “地沟油”禁止食用,但可以用来制肥皂 | |
| C. | 明矾常用于水体杀菌消毒 | |
| D. | 中秋将至,为防止月饼等富脂食品氧化变质,常在包装袋中放入生石灰 |
查看答案和解析>>
科目: 来源: 题型:计算题
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com