
科目: 来源: 题型:选择题
| A. | Cl2+H2O=HCl+HClO | B. | Fe+CuSO4=FeSO4+Cu | ||
| C. | 2NaHCO3 $\frac{\underline{\;△\;}}{\;}$Na2CO3+H2O+CO2 | D. | Cl2+2FeCl2=3FeCl3 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | FeS2既是氧化剂也是还原剂 | |
| B. | CuSO4在反应中被还原 | |
| C. | 14 mol CuSO4氧化了1 mol FeS2 | |
| D. | 被还原的S和被氧化的S的质量之比为3:7 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 一定条件下,1 molN2与足量的氢气反应合成氨,转移的电子数为6 NA | |
| B. | 常温下,1.0LpH=13的氢氧化钡溶液中OH-的数目为0.2NA | |
| C. | 常温常压下,4.6 g的NO2和N2O4混合物中,含原子总数一定为0.3NA | |
| D. | 1L0.1mol/L Na2CO3溶液中含CO32-数目为0.1NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 医院用碳酸钡代替硫酸钡做钡餐 | |
| B. | 生石灰,硅胶是食品包装中常用的干燥剂 | |
| C. | “雨后彩虹”是与胶体,光学等知识有关的自然现象 | |
| D. | 为防止月饼等富含脂食品氧化变质,常在包装袋中加入硫酸亚铁 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 向NaAlO2溶液中通入足量的CO2:2AlO${\;}_{2}^{-}$+CO2+3H2O=2Al(OH)3↓+CO${\;}_{3}^{2-}$ | |
| B. | (NH4)2Fe(SO4)2溶液中加入少量氢氧化钡溶液:NH${\;}_{4}^{+}$+SO${\;}_{4}^{2-}$+Ba2++OH-=BaSO4↓+NH3•H2O | |
| C. | NH4Cl浓溶液中滴加浓NaOH溶液并加热:NH${\;}_{4}^{+}$+OH-$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O | |
| D. | 磁性氧化铁溶于稀硝酸:3Fe2++4H++NO${\;}_{3}^{-}$=3Fe3++NO↑+2H2↑ |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
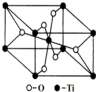 钛呈银白色,因它坚硬、强度大、耐热、密度小,被称为高技术金属.目前生产钛采用氯化法,即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:
钛呈银白色,因它坚硬、强度大、耐热、密度小,被称为高技术金属.目前生产钛采用氯化法,即将金红石或钛铁矿与焦炭混合,通入氯气并加热制得TiCl4:查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com