
科目: 来源: 题型:选择题
| A. | 食用白糖的主要成分是葡萄糖 | |
| B. | 淀粉溶液和蛋白质溶液都有丁达尔效应 | |
| C. | 油脂、淀粉和纤维素都是人体的重要营养物质 | |
| D. | 植物油的主要成分是高级脂肪酸 |
查看答案和解析>>
科目: 来源: 题型:选择题
 在一定温度和压强下,使Mg和Zn分别与等浓度、等体积的过量稀盐酸反应,产生气体的体积(V)与反应时间(t)的关系如图所示.下列叙述正确的是( )
在一定温度和压强下,使Mg和Zn分别与等浓度、等体积的过量稀盐酸反应,产生气体的体积(V)与反应时间(t)的关系如图所示.下列叙述正确的是( )| A. | 曲线a代表的是Zn的反应,曲线b代表的是Mg的反应 | |
| B. | 两个反应分别在2min、3min时达到化学平衡 | |
| C. | Mg和Zn的反应速率之比为3:2 | |
| D. | 用Fe代替Zn,其他条件不变,绘出的图象完全相同 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 化学反应释放或吸收能量的多少与发生反应的反应物的物质的量有关 | |
| B. | 人们可以利用氧化还原反应设计原电池以获取电能 | |
| C. | 人们可以利用C2H2(乙炔)与O2的化学反应获取热能或电能或光能 | |
| D. | MnO4-+5e-+8H+═Mn2++4H2O可能是某原电池里的负极反应 |
查看答案和解析>>
科目: 来源: 题型:实验题
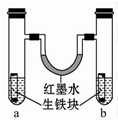 如图装置中,U形管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液(呈酸性),各加入生铁块,放置一段时间.
如图装置中,U形管内为红墨水,a、b试管内分别盛有食盐水和氯化铵溶液(呈酸性),各加入生铁块,放置一段时间.查看答案和解析>>
科目: 来源: 题型:选择题

| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 60g SiO2中含有NA个SiO2分子 | |
| B. | 标况下,22.4L SO3的分子数为NA | |
| C. | 1L 0.5 mol•L-1 CuCl2溶液中含有0.5NA个Cu2+ | |
| D. | 15.6 g Na2O2 与过量CO2反应时,转移的电子数为0.2NA |
查看答案和解析>>
科目: 来源: 题型:实验题
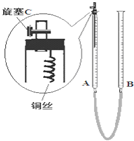 某实验小组同学探究铜与硝酸的反应.
某实验小组同学探究铜与硝酸的反应.| 序号 | 浓硝酸与水的体积比 | 实验现象 |
| Ⅰ | 1:1 | 反应速率快,溶液很快变成蓝色,大量气泡冒出,气体呈红棕色 |
| Ⅱ | 1:3 | 反应速率快,溶液变成蓝色,大量气泡冒出,气体呈无色 |
| Ⅲ | 1:5 | 反应速率慢,微热后加快,溶液变成蓝色,气泡冒出,气体无色 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com