
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量吸收液于试管中,滴加3moL•L-1 H2SO4至溶液呈酸性,然后将所得溶液分置于A、B试管中. | |
| 步骤2: | |
| 步骤3: |
查看答案和解析>>
科目: 来源: 题型:解答题
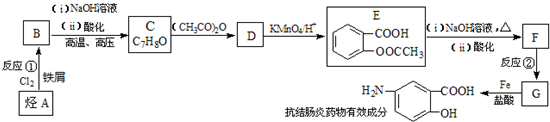
 $→_{盐酸}^{Fe}$
$→_{盐酸}^{Fe}$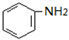 (苯胺易被氧化)
(苯胺易被氧化)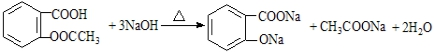 .
.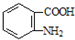 )合成路线中两种中间产物的结构简式(部分反应条件已略去)
)合成路线中两种中间产物的结构简式(部分反应条件已略去)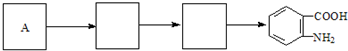
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na2O2可作漂白剂和供氧剂,碳酸钠可用于治疗胃酸过多 | |
| B. | 工业上用次氯酸制漂白粉,保存漂白粉的塑料袋要密封 | |
| C. | 氯气用于自来水消毒,是因为生成的次氯酸有杀菌、消毒的作用 | |
| D. | 溴化银用于人工降雨,单质碘加入食盐中用于制加碘盐 |
查看答案和解析>>
科目: 来源: 题型:填空题
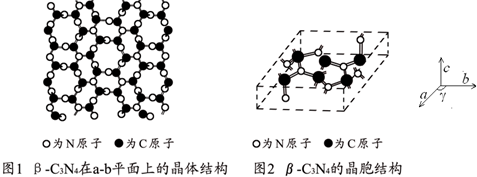
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 甘氨酸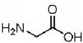 和硝基丙烷 CH3CH2CH2NO2互为同分异构体 和硝基丙烷 CH3CH2CH2NO2互为同分异构体 | |
| B. | 具有相同通式的两种有机物,要么互为同系物要么互为同分异构体 | |
| C. | C3H9N有四种 | |
| D. | 有机物中碳原子数一定时,烷烃中氢原子数最多 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 | |
| B. | 绿色化学的核心是利用化学原理治理环境污染 | |
| C. | 将煤气化或液化,获得清洁燃料 | |
| D. | 向高空排放金属冶炼产生的粉尘 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com