
科目: 来源: 题型:推断题
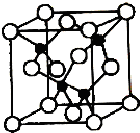 X、Y、Z、U、W是原子序数依次增大的前四周期元素.其中Y的原子核外有7种运动状态不同的电子;X、Z中未成对电子数均为2; U是第三周期元素形成的简单离子中半径最小的元素;W的内层电子全充满,最外层只有1个电子.请回答下列问题:
X、Y、Z、U、W是原子序数依次增大的前四周期元素.其中Y的原子核外有7种运动状态不同的电子;X、Z中未成对电子数均为2; U是第三周期元素形成的简单离子中半径最小的元素;W的内层电子全充满,最外层只有1个电子.请回答下列问题:查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 3.2mol/L | B. | 1.6mol/L | C. | 0.9mol/L | D. | 无法判断 |
查看答案和解析>>
科目: 来源: 题型:解答题
| X | Y | Z | M | R | Q | |
| 原子半径/nm | 0.186 | 0.074 | 0.099 | 0.143 | ||
| 主要化合价 | -4,+4 | |||||
| 其他 | 阳离子 核外无电子 | 无机非金属材料的主角 | 焰色反 应呈黄色 |
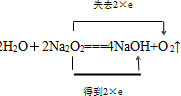 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ①②④⑤ | B. | ②③⑤ | C. | ②③④⑦ | D. | 全部 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | CO2+2OH-=CO32-+H2O | B. | Al2O3+2OH-=2 AlO2-+H2O | ||
| C. | 2 Al+2OH-+2H2O=2 AlO2-+3H2↑ | D. | Al3++4 OH-=AlO2-+2H2O |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 115mol/L | B. | 1mol/L | C. | 3mol/L | D. | 2mol/L |
查看答案和解析>>
科目: 来源: 题型:解答题
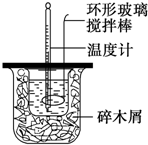 50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.
50mL 0.50mol•L-1盐酸与50mL 0.55mol•L-1NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.查看答案和解析>>
科目: 来源: 题型:实验题
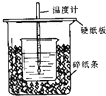 50mL0.50mol/L 盐酸与50mL0.55mol/LNaOH 溶液在如图所示的装置中进行中和反应.
50mL0.50mol/L 盐酸与50mL0.55mol/LNaOH 溶液在如图所示的装置中进行中和反应.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com