
科目: 来源: 题型:选择题
| A. | 取代,4 mol Cl2 | B. | 加成、取代,3 mol Cl2 | ||
| C. | 加成,2 mol Cl2 | D. | 加成、取代,5 mol Cl2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 金属元素原子最外层电子数越少,该金属失电子能力越强 | |
| B. | 铅位于周期表中金属和非金属的交界处,可作半导体材料 | |
| C. | aA2+、bB+、cC3-三种离子具有相同的电子层结构,则原子序数c>a>b | |
| D. | 若存在简单阴离子R2-,则R一定位于ⅥA族 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1:1:1 | B. | 1:4:2 | C. | 1:2:4 | D. | 1:3:2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1.2g | B. | 1.6g | C. | 2.4g | D. | 4.8g |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 图①是向一定量的稀盐酸和氯化钙的混合溶液中不断滴入碳酸钠溶液至过量 | |
| B. | 图②是用H2还原CuO来测定CuO中铜元素的含量 | |
| C. | 图③是向饱和的NaCl溶液中不断加水 | |
| D. | 图④是用适量的KClO3和MnO2混合物加热制O2 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温常压下,17g甲基(-14CH3)所含的中子数为8NA | |
| B. | 0.1molFe与0.1molCl2充分反应,转移的电子数为0.2NA | |
| C. | 标准状况下,44.8LNO与22.4LO2混合后气体的分子总数为2NA | |
| D. | 1molNa2O和Na2O2混合物中含有的阴、阳离子总数是3NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在含大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| B. | Na2S溶液中:SO42-、K+、Cl-、Cu2+ | |
| C. | 0.1 mol•L-1 NH4HCO3溶液中:K+、Na+、NO3-、Cl- | |
| D. | 在溶质为KNO3和NaHSO4的溶液中:Fe2+、Ca2+、Al3+、Cl- |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ${\;}_{53}^{131}$I放出射线是一个自发的化学变化过程,射线对人危害很大 | |
| B. | 不同元素的原子构成的分子只含极性共价键 | |
| C. | H2和T2是两种不同的物质,互称为同位素 | |
| D. | 短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
查看答案和解析>>
科目: 来源: 题型:实验题
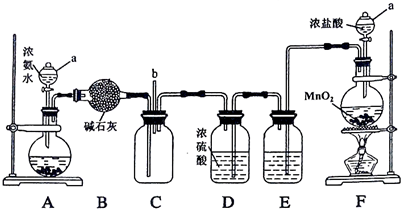
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com