
科目: 来源: 题型:选择题
| A. | 硅胶可以用作干燥剂、催化剂 | |
| B. | 为加快漂白粉的漂白速率,可加氢氧化钠 | |
| C. | 氯化铁水解可以制备胶体,所以常用于杀菌消毒 | |
| D. | 淀粉和水可以检验出食盐中含碘 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na2O+H2O═2NaOH | B. | Cl2+H2O═HCl+HClO | ||
| C. | H2SO4+Na2SO3=Na2SO4+SO2↑+H2O | D. | FeS+2HCl═FeCl2+H2S↑ |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 仅①③ | B. | 仅②③ | C. | 仅①② | D. | 仅③ |
查看答案和解析>>
科目: 来源: 题型:解答题
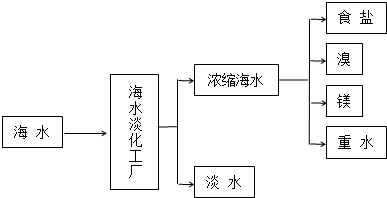
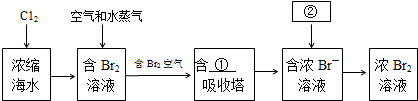
查看答案和解析>>
科目: 来源: 题型:解答题

查看答案和解析>>
科目: 来源: 题型:解答题
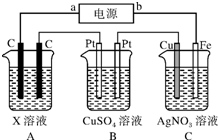 如图所示,电解一段时间后,测得C中Ag+减少了0.1mol,Fe电极被溶解.试回答:
如图所示,电解一段时间后,测得C中Ag+减少了0.1mol,Fe电极被溶解.试回答:查看答案和解析>>
科目: 来源: 题型:推断题
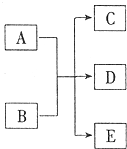 一定条件,物质A~E转化关系如图,其中A为单质,常温下E为无色液体.
一定条件,物质A~E转化关系如图,其中A为单质,常温下E为无色液体.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com