
科目: 来源: 题型:选择题
| A. | 稀盐酸 | B. | 稀NaOH溶液 | ||
| C. | FeCl3溶液 | D. | 酸性高锰酸钾溶液 |
查看答案和解析>>
科目: 来源: 题型:多选题
| A. | 加入适量的水 | B. | 适当升高温度 | ||
| C. | 加入少量CuSO4溶液 | D. | 加入等体积的浓度较大的盐酸 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 元素Y、Z、W具有相同电子层结构的离子,其半径依次增大 | |
| B. | 元素Y能与元素Z形成化合物Z2Y2,该化合物内部有两种化学键 | |
| C. | 元素Y、R分别与元素X形成的化合物的热稳定性:XmY>XmR,沸点XmY<XmR | |
| D. | 元素W、R的最高价氧化物的水化物都是强酸 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:解答题
 氧化铜是一种黑色粉末,可作玻璃和瓷器着色剂、油类的脱硫剂、有机合成的催化剂.为获得纯净的氧化铜以探究其性质,某化学兴趣小组利用废旧印刷电路板获得氧化铜,实现资源再生,并减少污染.
氧化铜是一种黑色粉末,可作玻璃和瓷器着色剂、油类的脱硫剂、有机合成的催化剂.为获得纯净的氧化铜以探究其性质,某化学兴趣小组利用废旧印刷电路板获得氧化铜,实现资源再生,并减少污染.| 实验序号 | Ⅰ | Ⅱ | Ⅲ |
| KClO3质量 | 1.2g | 1.2g | 1.2g |
| 其他物质质量 | 无其他物质 | CuO 0.5g | MnO2 0.5g |
| 待测数据 |
查看答案和解析>>
科目: 来源: 题型:解答题
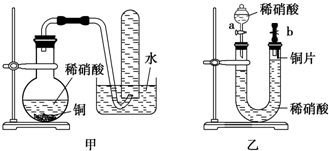
 实验室用稀硝酸与铜反应来制备NO气体,如果采用(Ⅰ)装置(烧瓶内加入稀硝酸和铜片,必要时可加热),实验效果不十分理想,因为从观察到的现象不能有力证明反应产物是NO;有人设计了(Ⅱ)装置(橡皮塞下端连有铜丝圈),用来做该实验可以达到满意的效果.根据要求回答下列问题:
实验室用稀硝酸与铜反应来制备NO气体,如果采用(Ⅰ)装置(烧瓶内加入稀硝酸和铜片,必要时可加热),实验效果不十分理想,因为从观察到的现象不能有力证明反应产物是NO;有人设计了(Ⅱ)装置(橡皮塞下端连有铜丝圈),用来做该实验可以达到满意的效果.根据要求回答下列问题:查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:选择题
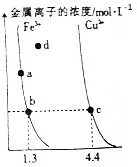
| A. | Ksp[Fe(OH)3]<Ksp[Cu(OH)2] | |
| B. | a、b、c、d四点的Kw不同 | |
| C. | 在Fe(OH)3饱和溶液中加入适量硝酸钾晶体可使a点变到b点 | |
| D. | d点时的Cu(OH)2溶液为不饱和溶液 |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com