
科目: 来源: 题型:选择题
| A. | 在反应3Br2+3CO32-=5Br-+BrO3-+3CO2↑中,每生成3 mol CO2转移的电子数为5NA | |
| B. | 0.5 mol 甲基中电子数为5NA | |
| C. | 常温下,1 L 0.1 mol/L的NH4NO3溶液中氢原子总数为0.4NA | |
| D. | 常温常压下,22.4 L N2H4中N-H键数为4NA |
查看答案和解析>>
科目: 来源: 题型:解答题
查看答案和解析>>
科目: 来源: 题型:实验题
查看答案和解析>>
科目: 来源: 题型:实验题
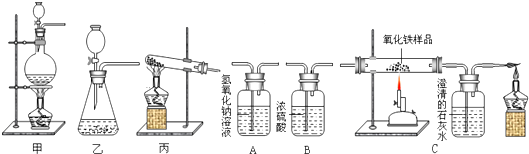
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 在演示实验和分组实验中,要力求利用最少的实验用品,获得最佳的实验效果,最大限度的减少废弃物 | |
| B. | 稀释浓硫酸时,应沿烧杯壁向浓硫酸中缓缓加水,并用玻璃棒不断搅拌 | |
| C. | 取用液体药品时,要把瓶塞反放在桌面上,标签朝向手心,放回原处时标签向外 | |
| D. | 不能用手接触实验室里的药品,不要凑到容器口闻气体的气味 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 常温下4.4gN2O与标准状况下2.24LCH4均含有0.1NA个分子 | |
| B. | 78g金属钾(K)完全转化为超氧化钾(KO2)时,转移电子数为4NA | |
| C. | 0.1mol/L稀盐酸中,H+数目为0.1NA | |
| D. | 60g二氧化硅晶体中,含S-O键数目为2NA |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | NaOH溶液中混有Ba(OH)2(CuSO4) | B. | Cu(NO3)2溶液中混有AgNO3(Cu粉) | ||
| C. | 氧化铜中混有少量的铜粉(稀硫酸) | D. | NaCl溶液中混有BaCl2(CO2) |
查看答案和解析>>
科目: 来源: 题型:选择题

| A. | 该硫酸的物质的量浓度为18.4 mol/L | |
| B. | 该硫酸常用做干燥剂 | |
| C. | 配制200 mL 4.6 mol/L的稀硫酸需取该硫酸50 mL | |
| D. | 该硫酸与等质量的水混合后所得溶液的浓度大于9.2 mol/L |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 单位时间内生成n mol H2,同时生成n mol I2 | |
| B. | 容器内压强不随时间而变化 | |
| C. | 单位时间内生成2n mol HI,同时生成n mol I2 | |
| D. | 混合气体的平均分子量不随时间而变化 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为$\frac{7}{22.4}$NA | |
| B. | 1 mol甲基(-CH3)所含的电子总数为9NA | |
| C. | 0.5 mol1,3-丁二烯分子中含有C=C双键数为 NA | |
| D. | 28g乙烯所含共用电子对数目为6NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com