
科目: 来源: 题型:实验题
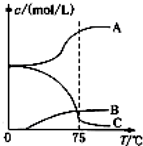 氯酸钠(NaClO3)是无机盐工业的重要产品之一.
氯酸钠(NaClO3)是无机盐工业的重要产品之一.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 10-11mol/L | B. | 10-3mol/L | C. | 10-7mol/L | D. | 0.1 mol/L |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 分子数之比为1:1 | B. | 密度之比为3:2 | ||
| C. | 质量之比为7:11 | D. | 质子数之比为7:11 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 胶体和溶液的本质区别是胶体可以发生丁达尔现象 | |
| B. | 0.1molFeCl3溶于水中形成胶体后含有胶体粒子的数目为0.1NA | |
| C. | 明矾净水与胶体的性质有关 | |
| D. | 可以用滤纸分离提纯胶体和溶液 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 将固体加入容量瓶中溶解并稀释至刻度线,配制成一定物质的量浓度的溶液 | |
| B. | 稀释硫酸时,往装有浓硫酸的烧杯中注入水 | |
| C. | 用托盘天平称取10.600 g的Na2CO3固体,溶于1 L的水可配成0.1 mol/L的溶液 | |
| D. | 容量瓶中残留少量蒸馏水时,无需干燥,对配制的结果没有影响 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | Na2O、Na2O2、CaO均属于碱性氧化物 | |
| B. | H2和HD属于同素异形体 | |
| C. | 蓝色的硫酸铜晶体遇到浓硫酸变白色属于化学变化 | |
| D. | 胶体带电,所以胶体具有电泳的性质 |
查看答案和解析>>
科目: 来源: 题型:解答题
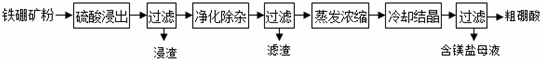
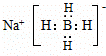 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 标准状况下,22.4L盐酸含有NA个HCl分子 | |
| B. | 常温常压下,22.4L CO2和SO2混合气体含有2NA个O原子 | |
| C. | 常温常压下,8g CH4的体积为11.2L | |
| D. | 标准状况下,22.4L的H2和CO2混合气体中含有的分子总数为NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com