
科目: 来源: 题型:选择题
| A. | 3-甲基-2-乙基戊烷 | |
| B. | (CH3)3CCH2CH(C2H5)CH3 2,2-二甲基-4-乙基戊烷 | |
| C. | 2-甲基-3-戊炔 | |
| D. | 邻甲基苯酚 |
查看答案和解析>>
科目: 来源: 题型:选择题
 ,这种炔烃的名称为( )
,这种炔烃的名称为( )| A. | 5-甲基-3-乙基-1-己炔 | B. | 5-甲基-3-乙基-2-己炔 | ||
| C. | 4-甲基-5-乙基-2-己炔 | D. | 2-甲基-4-乙基-5-己炔 |
查看答案和解析>>
科目: 来源: 题型:填空题
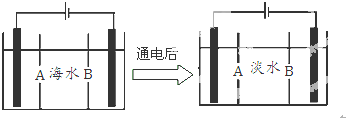
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | [Na+]>[A-]>[H+]>[OH-] | B. | [Na+]>[OH-]>[A-]>[H+] | C. | [Na+]+[OH-]=[A-]+[H+] | D. | [Na+]+[H+]=[A-]+[OH-] |
查看答案和解析>>
科目: 来源: 题型:解答题
| 滴定 次数 | 待测溶液的体积/mL | 标准溶液的体积/mL | |
| 滴定前刻度 | 滴定后刻度 | ||
| 1 | 25.00 | 1.02 | 21.03 |
| 2 | 25.00 | 2.00 | 20.80 |
| 3 | 25.00 | 0.20 | 20.19 |
查看答案和解析>>
科目: 来源: 题型:推断题
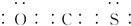 .
. HSO3-+OH-;溶液中离子浓度由大到小的顺序为c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+).
HSO3-+OH-;溶液中离子浓度由大到小的顺序为c(Na+)>c(SO32-)>c(OH-)>c(HSO3-)>c(H+).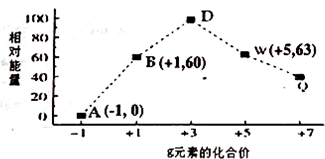
查看答案和解析>>
科目: 来源: 题型:解答题
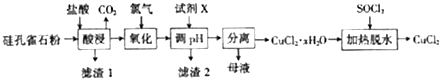
 .
.查看答案和解析>>
科目: 来源: 题型:选择题
| A. | 1:2:3 | B. | 4:3:3 | C. | 8:6:9 | D. | 1:1:1 |
查看答案和解析>>
科目: 来源: 题型:选择题
| A. | ②③ | B. | ②③④⑤ | C. | ①③⑤ | D. | ①③④⑤ |
查看答案和解析>>
科目: 来源:2017届江西省高三上第二次月考化学试卷(解析版) 题型:选择题
美国宇航局“凤凰”号火星登陆器的显微、电子化学及传导分析仪对两份土壤样本的分析发现,火星 北极区表层土壤可能含有高氯酸盐,可创造不利于任何潜在生命的恶劣环境。则下列说法正确的是
北极区表层土壤可能含有高氯酸盐,可创造不利于任何潜在生命的恶劣环境。则下列说法正确的是
A.含有高氯酸盐的土壤不利于生命存在与高氯酸盐具有较强的还原性有关
B.当元素处于最高价态时一 定具有强氧化性
定具有强氧化性
C.可以考虑用加入亚铁盐等还原性物质的方法改善这种土壤
D.高氯酸盐与浓盐酸反应一定只能生成氯气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com